双模态成像新突破:于法标团队开发生物正交 SERS - 生物发光探针追踪三阴乳腺癌转移
3月16日,急救与创伤教育部重点实验室/急诊创伤学院于法标教授团队在《Acta Biomaterialia》上发表了题为“Bioorthogonal SERS-Bioluminescence Dual-Modal Imaging for Real-Time Tracking of Triple-Negative Breast Cancer Metastasis”的研究成果。

原文链接:https://doi.org/10.1016/j.actbio.2025.03.019
三阴性乳腺癌 (TNBC) 是一种侵袭性乳腺癌亚型,其特征是早期转移和预后不良。常规成像技术缺乏检测早期转移性病变的灵敏度和分子特异性。在此,我们开发了一种双模态成像策略,即表面增强拉曼散射 (SERS) 和生物发光成像探针集成生物正交标记来追踪 TNBC 器官转移。SERS 探针被叠氮化物标记的巨噬细胞膜包裹,以延长循环时间并提高靶向效率。采用生物正交糖代谢工程用双环 [6.1.0] 壬炔 (BCN) 基团修饰荧光素酶标记的肿瘤细胞 (4T1-Luc),通过点击化学反应促进探针与 4T1-Luc 细胞之间的精确结合。提出的双模态成像策略可以灵敏地实时监测小转移性病变,为体内监测肿瘤转移和治疗反应提供了一种非侵入性、准确的方法。本研究结果表明,SERS 和生物发光双模成像与生物正交标记相结合,对于促进转移性癌症的早期检测和治疗监测具有巨大潜力。
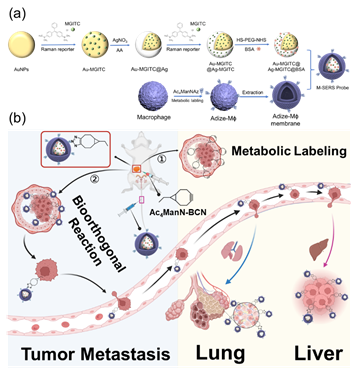
图1. 生物正交标记用于通过SERS和生物发光成像实时追踪三阴性乳腺癌(TNBC)肿瘤转移的示意图。
三阴性乳腺癌(TNBC)是一种高度侵袭性的乳腺癌亚型,其特征是缺乏雌激素受体、孕激素受体以及人类表皮生长因子受体2(HER2)的过表达。这种亚型由于其快速进展和早期向重要器官(如肺、肝和脑)转移的倾向而带来了重大挑战。TNBC的转移与不良预后和有限的治疗选择相关,因此迫切需要开发有效的监测策略以实现早期检测和干预。如果能够监测甚至通过药物阻断早期肿瘤转移,患者的预后将得到显著改善。
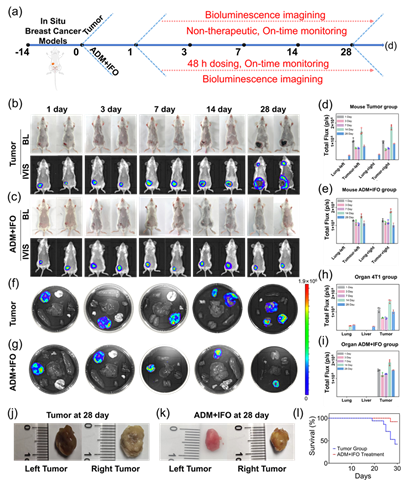
图2. (a) 示意图显示了体内生物发光成像和药物治疗评估的实验设计;(b) 上排为三阴性乳腺癌组的照片图像。下排为三阴性乳腺癌组在第1 d、第3 d、第7 d、第14 d和第28 d的生物发光图像(每组n = 2只小鼠)。(c) 上排为阿霉素(ADM)+异环磷酰胺(IFO)治疗组的照片图像。下排为ADM + IFO治疗组在第1天、第3天、第7天、第14天和第28天的生物发光图像(每组n = 2只小鼠)。(d) 和 (e) 分别为(b)和(c)中重要器官的平均生物发光信号强度的量化分析。(f) 和 (g) 分别为肿瘤组和治疗组的体外生物发光图像,包括肿瘤、肝脏和肺部。(h) 和 (i) 分别为(f)和(g)中肿瘤和重要器官的平均生物发光信号强度的量化分析。所有生物发光信号均在560 nm波长下采集。(j) 和 (k) 分别为第28天有无药物治疗的肿瘤大小。(l) 为有无ADM + IFO治疗的小鼠模型的Kaplan-Meier生存曲线。生存曲线分析采用Log-rank(Mantel-Cox)检验。
在本研究中,我们提取了叠氮基标记的巨噬细胞膜(MϕM)来封装SERS探针,以延长其循环时间并增加其在肿瘤中的有效积累。叠氮基通过糖代谢处理叠氮糖Ac4ManNAz标记在巨噬细胞膜上。荧光素酶标记的肿瘤细胞(4T1-Luc)通过先前瘤内注射的BCN糖Ac4ManNBCN进行天然糖代谢携带BCN基团。Au@Ag核壳纳米粒子固定了双层拉曼报告分子,并与HS-PEG结合后涂覆BSA形成SERS探针,然后用提取的叠氮基标记巨噬细胞膜封装,形成叠氮基标记的MϕM封装SERS探针(M-SERS探针)。通过将巨噬细胞膜转移到SERS探针上,M-SERS探针可以抑制巨噬细胞的吞噬作用,这有助于通过减少不利清除延长其在血液循环中的时间。此外,叠氮基和BCN基团之间的生物正交反应可以显著增强M-SERS探针的锚定效果。SERS和生物发光双模态成像实现了对TNBC器官转移的实时和精确追踪,尤其是对小型转移病灶。
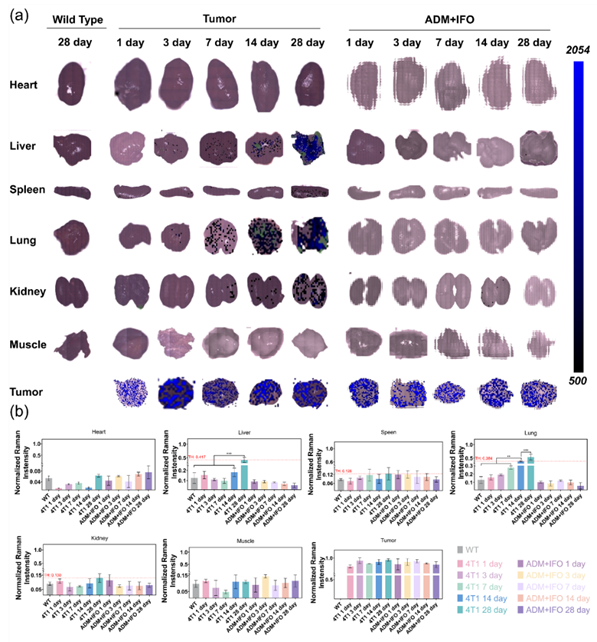
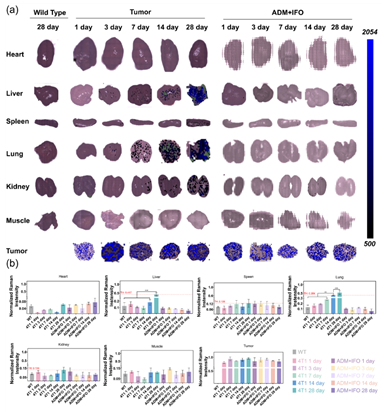
图3. (a) 野生型小鼠、三阴性乳腺癌小鼠模型组和药物治疗小鼠模型组在不同时间点(第1 d、第3 d、第7 d、第14 d和第28 d)的肿瘤和重要器官的SERS成像。(b) 在野生型、肿瘤组和治疗组中分别应用M-SERS探针后的SERS信号强度量化。SERS映射使用0.5 s的曝光时间完成(633 nm激光功率,50 × 物镜)。统计分析采用单因素方差分析后进行Tukey多重比较(n = 3,平均值 ± 标准误,**P < 0.01,***P<0.001)。
该研究成果以海南医科大学为第一单位,我校青年教师张伟,硕士研究生王思厶为共同第一作者,于法标教授、王锐教授担任共同通讯作者。该研究受到省重研发和国家自然科学基金项目资助。

