
体内表面增强拉曼散射技术:纳米探针、仪器与应用
In vivo surface-enhanced Raman scattering techniques: nanoprobes, instrumentation, and applications
论文信息:Hyejin Chang, Won Hur, Homan Kang & Bong-Hyun Jun
主讲人:李世伟,2025年12月07日
研究进展:
1.传统临床成像技术(CT、PET、MRI、超声等)存在局限性:CT/PET 有电离辐射风险,MRI/PET 成本高、空间分辨率不足,超声 / CT 缺乏多重检测能力,难以满足精准诊疗需求。
2.表面增强拉曼散射(SERS)技术凭借非侵入性、高特异性、信号稳定等优势兴起,近红外(NIR)窗口(NIR-I:650-900 nm;NIR-II:1000-1700 nm)的应用解决了生物组织对可见光的强吸收、自荧光及散射问题,大幅提升成像深度与灵敏度。
3.关键里程碑研究奠定基础:2006 年实现体内葡萄糖无标记 SERS 检测,2008 年完成靶向纳米探针的肿瘤无创检测,后续多重检测技术突破推动 SERS 向临床转化。
研究内容:
(一)SERS 纳米探针设计
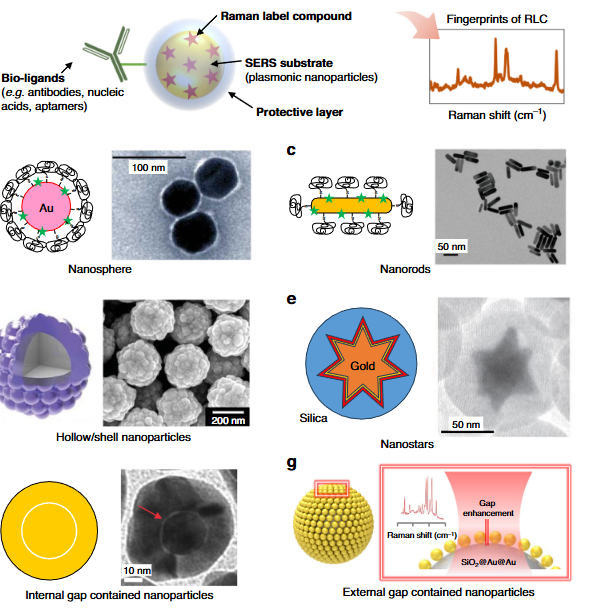
1.核心组件:包括 plasmonic 纳米基底(Au/Ag 纳米球、纳米棒、纳米星等)、拉曼标记化合物(RLCs)、保护层(PEG、二氧化硅等)及生物配体(抗体、适配体等)。
2.优化方向:通过调控基底形貌(如各向异性纳米棒、带 “热点” 的纳米星)匹配 NIR 窗口,选用高拉曼截面的 RLCs(如近红外染料衍生物),修饰保护层提升生物相容性与稳定性,偶联生物配体实现靶向识别。
(二)仪器配置优化
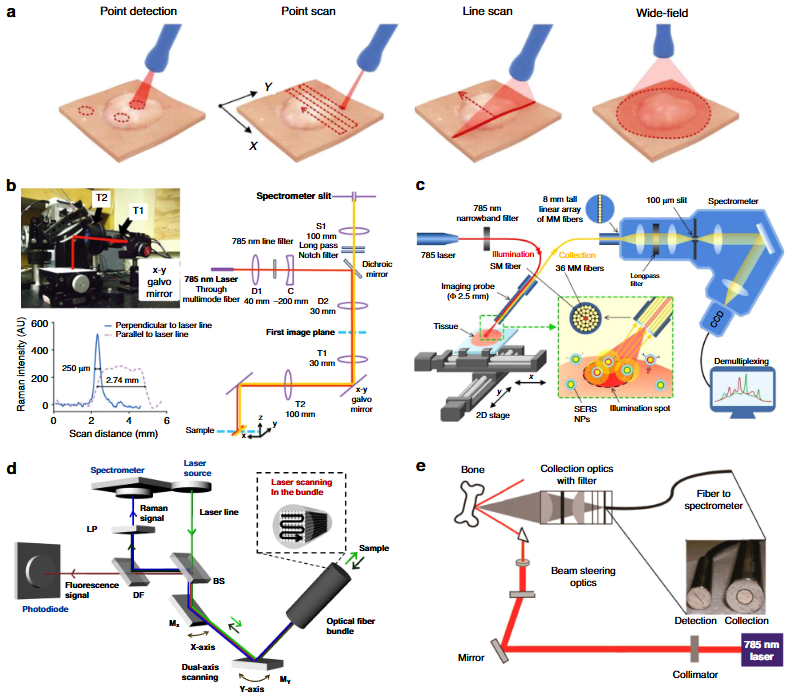
1.显微镜基配置:涵盖点扫描、线扫描(如 SARI 系统)、宽场成像,适配不同成像范围与分辨率需求,核心参数包括 785 nm/1064 nm 激发激光、Si/InGaAs 探测器。
2.光纤基配置:包括内窥镜、手持探针(如 SpectroPen)、空间偏移拉曼光谱(SESORS),满足术中导航、深部组织检测等微创 / 无创场景需求。
(三)体内核心应用
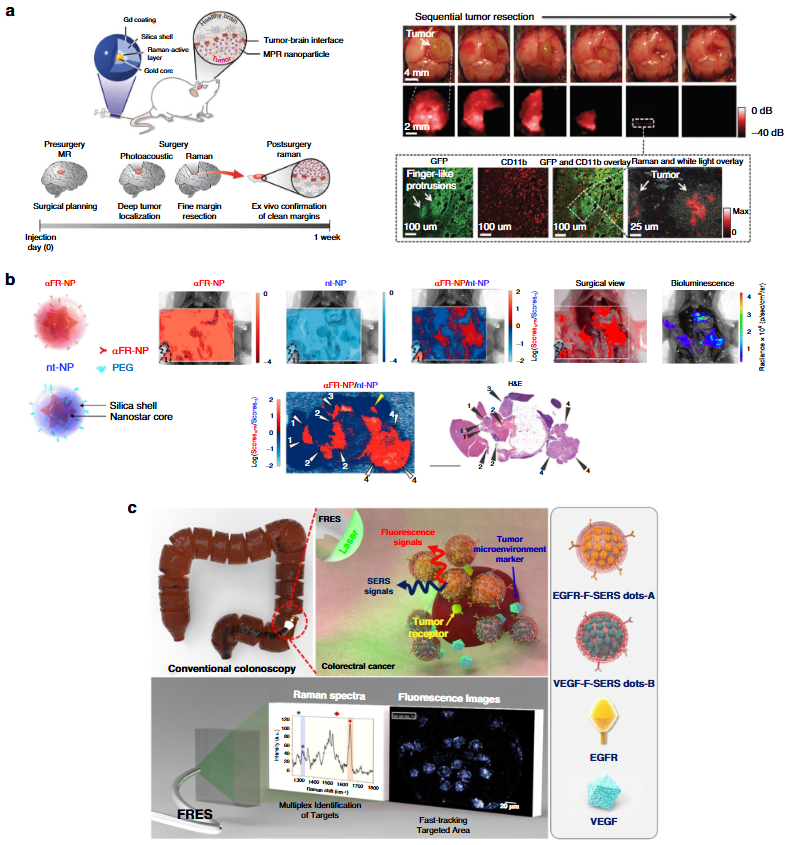
1.传感与诊断:实现葡萄糖、神经递质等生物分子的非侵入检测,以及植物胁迫信号分子、肿瘤标志物的精准识别。
2.生物分子筛选与多重成像:利用 SERS 窄光谱特性,实现多靶点同步检测,助力药物筛选与肿瘤异质性分析。
3.术中导航:通过靶向纳米探针精准勾勒肿瘤边界,结合拉曼成像引导手术切除,降低残留风险。
4.多功能癌症治疗:整合光热治疗(PTT)、化疗的纳米探针,实现 “成像 - 治疗” 一体化。
要点:
1.纳米探针是核心:基底的等离子体共振调控、RLCs 的信号增强能力、保护层的生物相容性,直接决定检测灵敏度与体内适用性。
2.仪器适配场景:显微镜基系统适用于预临床大视野成像,光纤基系统适配临床微创 / 术中检测,需根据应用场景选择激发波长与探测器。
3.技术优势显著:相比传统技术,SERS 具备多重检测能力、低背景噪音、微创 / 无创特性,在精准医疗中具有不可替代的价值。
4.临床转化关键挑战:需解决纳米探针的生物安全性(毒性、代谢)、检测重复性、仪器成本控制,以及穿透深度优化(NIR-II 窗口潜力更大)
总结与展望:
1.总结:SERS 技术通过纳米探针优化与仪器创新,已在体内传感、肿瘤诊疗、术中导航等领域取得突破性进展,成为连接基础研究与临床应用的关键技术。其核心优势在于高特异性、多重检测能力及 “成像 - 治疗” 一体化潜力,弥补了传统成像技术的短板。
2.展望:未来需重点推进 NIR-II 窗口纳米探针的临床转化,优化生物相容性与代谢途径;结合 AI / 机器学习提升数据解析效率;开发多模态成像系统(如 SERS-MRI / 光声成像);建立标准化检测流程,降低仪器成本,推动 SERS 技术在个性化医疗、早期疾病诊断中的广泛应用。

