所谓眼见为实,人类通过感官从自然界获取的各种信息中,以视觉信息占比最高,约占获取信息总量的80%。然而人眼的分辨率极限为100 μm左右,大概是一根头发的直径,因此仅能对宏观尺度生物个体及器官、组织进行观察,但无法直接观察细胞、亚细胞等微观世界的生命活动。17世纪,列文虎克和罗伯特·胡克对光学显微镜的创造性贡献及应用,为人类提供了探索生命活动微观世界大门的钥匙,光学显微镜具备对微米尺度的细菌、细胞及其内部结构进行观察的能力(图1)[1]。
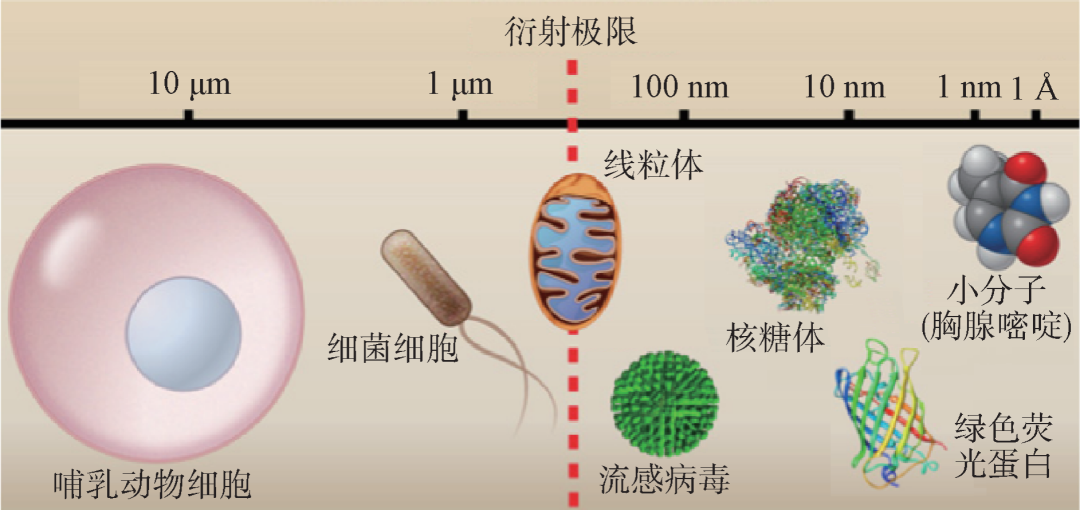
图1 不同生物样品尺寸与衍射极限比较[1]
深入研究细胞的生命活动,需要提高显微镜的分辨率和成像衬度这两个关键指标。要观察细胞内的精细结构,最重要的是分辨率。分辨率是指能区分的两个点之间的最小距离(图2)。一个理想的点光源在通过显微镜的透镜系统后,其光束会聚集成一个微小的光斑。在这个过程中,由于光的衍射现象,光斑的大小会随着波长和显微镜数值孔径而变化。当两个光斑靠得太近时,他们之间的界限变得模糊不清,从而无法分辨出它们各自的位置。这种现象导致了显微镜存在一个分辨率极限。换句话说,如果两个点光源的距离小于分辨率极限,我们就无法分辨出两个物体。因此,分辨率极限是光学显微镜的一个重要限制因素,它限制了显微镜能够分辨出的最小物体的尺寸。

图2 衍射极限的概念(图片来自维基百科)
19世纪,以德国物理学家阿贝为代表的研究者通过各种方式大幅改善了显微镜的分辨率,如利用油镜来增加物镜的数值孔径,采用更好的像差校正技术来设计显微镜的光学系统等。然而阿贝也于1873年提出,显微镜的分辨率受到光学衍射极限的限制[2],横向和轴向分辨率理论极限分别由下式所决定:
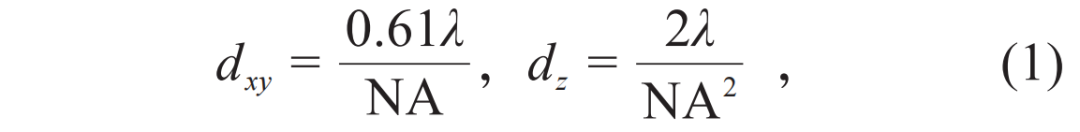
其中,dxy和dz分别表示传统光学显微镜的横向、轴向分辨率,λ表示光的波长,NA表示所使用物镜的数值孔径。由此可见,在可见光波段(400—700 nm),传统光学显微镜的横向分辨率只能达到200—300 nm,轴向分辨率极限在500—800 nm。也就是说,如果两个目标之间的距离小于两三百纳米,我们便无法区分它们。由于很多亚细胞结构如细胞骨架、细胞器、细胞内膜结构等都在数纳米到数百纳米的尺度,因此用传统显微镜难以对其进行研究。
除了分辨率,衬度也是显微镜成像重要的指标。细胞对可见光有较高的透过率,以更高的对比度观察细胞是细胞生物学研究中亟待解决的问题。为了解决这个问题,科学家们采用了许多技术手段来增强显微镜下细胞的对比度。20世纪相衬显微镜和微分干涉显微镜的提出,为生物学和医学领域带来了重大的突破,使得我们能够观察到透明细胞的细节[3,4]。这两种成像技术通过将细胞内微小的折射率变化转换成可见的亮度变化,从而使观察透明细胞的微小结构成为可能。
另一项革命性的技术是荧光标记以及荧光显微镜技术。这种技术利用特殊的荧光染料或荧光蛋白标记细胞中的特定结构或蛋白质,从而使其在显微镜下更容易被发现。随着荧光标记技术在20世纪被发明,将细胞特定结构标记上荧光探针,就能清晰地观察各种亚细胞结构。与传统的染色技术不同,荧光标记具有高灵敏度、高特异性和高分辨率等优点,可以清晰地观察各种亚细胞结构,包括细胞器、细胞膜、染色体等。荧光成像具有非常高的对比度,配合高灵敏光学检测系统,甚至可以实现单个荧光分子信号的检测。通过将特定蛋白连接荧光分子,可以在细胞内对单个蛋白进行定位和追踪,这在之前是无法实现的。荧光显微镜为研究亚细胞结构和生物大分子功能供了强有力的工具。
荧光标记技术也推动了显微镜技术的发展,20世纪50年代发明的共聚焦显微镜(confocal laser scanning microscope,CLSM)[5],通过将光束汇聚成一个小点来扫描样品,并通过一个针孔过滤背景荧光,从而实现光学层析成像。它可以利用点扫描技术获得细胞或组织三维图像,提高图像的清晰度和分辨率,克服了普通荧光显微镜成像模糊、三维分辨率低的缺点。它的发明标志着光学显微成像技术进入了高清三维成像时代。
进入21世纪以来,多种超高分辨率荧光成像技术相继被提出,打破了光学衍射极限。其中最具代表性的三种技术分别是受激发射损耗显微镜(stimulated emission depletion,STED)、结构光照明显微镜(structured illumination microscopy,SIM)和单分子定位显微镜(single molecule localization microscopy,SMLM)。
STED的概念最早由德国马普所的Stefan W. Hell教授于1994年提出,它采用点扫描的方式成像,将激发光(图3(a)绿色光路)和中心光强为零的环形损耗光(红色光路)同时聚焦在样品上[6]。由于荧光分子受激发射产生的信号波长与损耗光相同,可以被滤光片滤掉,因此探测器接收到的被绿光激发的荧光信号(黄色光路)就是损耗光中心光强为零的区域的信号。使用这种方法,可以将等效的成像区域尺寸缩小到衍射极限以下,实现超分辨成像(图3(b))。STED的分辨率可以到数十纳米[7—9]。
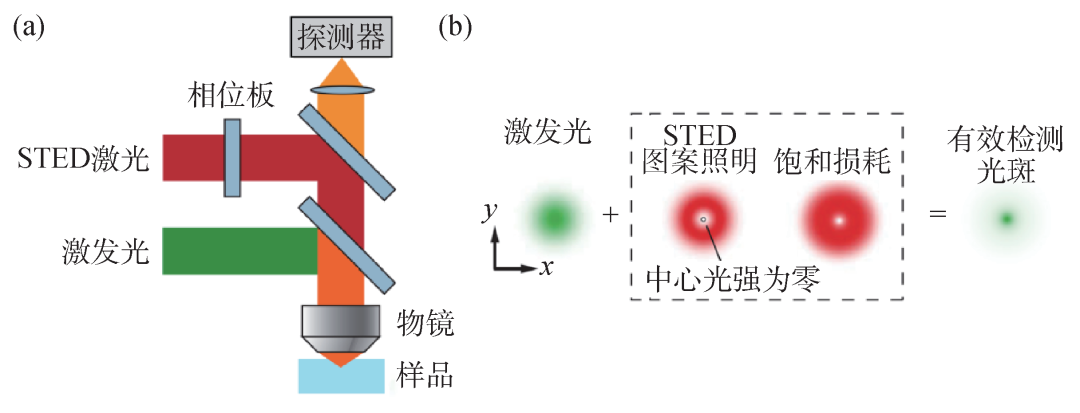
图3 (a)STED技术所用成像光路;(b)STED原理图[6]
SIM是一种基于面照明和相机检测的成像技术,通过将目标的高频信息移到低频部分上,拓宽了可以被显微镜系统捕获的空间频率范围,进而实现样品结构细节的解析。在光学显微成像中,由于物镜的收集能力限制,样品的高频信息会被丢失,无法被显微镜捕获和记录。SIM技术通过莫尔条纹的叠加,可以将这些位于物镜收集能力范围之外的高频信息“搬运”到低频区域,从而让显微镜能够捕获到这些原本无法获取的信息(图4)。

图4 SIM技术原理[10]。未知样品的高频信息表现为细条纹,当未知样品与已知结构光照明图案相重叠,未知样品的高频信息被移到低频处,表现为较宽的条纹
在采集结构光照明的样品图像后,SIM技术采用特殊的图像算法处理这种叠加的低频信息和高频信息,从而获取超分辨图像。这种超分辨图像的分辨率能够比普通光学显微镜提高一倍左右[10,11]。SIM技术的优势是能够在极低光强下实现超分辨率成像,它在时间分辨率以及低光毒性等方面有独特的优势。因此非常适合针对活细胞动态过程的长时间观察。
SMLM的技术原理是,对一个单分子的位置测量的误差可以远远小于其光斑的尺寸,因此如果可以对样品中所有荧光分子的位置进行重构,就可以突破衍射限制,实现对细胞内纳米结构更高的分辨能力。
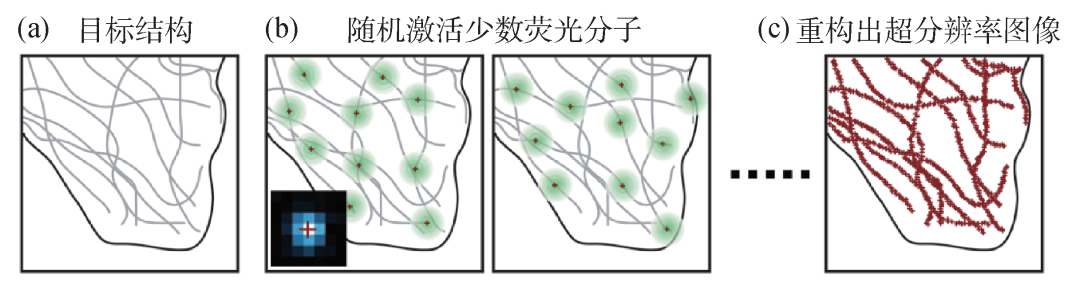
图5 SMLM技术原理[9] (a)生物样品中目标结构被荧光分子标记;(b)通过随机激活少量荧光分子,实现对样品中单分子信号的采集,用绿色光斑表示,单分子定位得到的位置信息使用红色十字表示;(c)通过对多帧图像得到的单分子定位数据进行重构,解析出超分辨率图像
这种技术同样是使用面照明和相机检测,其侧向(XY)分辨率可达20 nm左右。该技术自2006年提出以来得到快速发展,和STED技术一起于2014年获得诺贝尔化学奖。其核心在于利用光控荧光分子的随机发光性质,在单帧图像上获得空间上互相独立的单个荧光分子的图像,通过单分子图像识别及质心拟合算法,对每个单分子进行精确定位。此外,该技术利用时间换空间的方式,通过采集数万张稀疏分布的单分子图像,获得组成目标结构的大部分分子位置,并将这些分子位置信息叠加,最终重构出超分辨率的图像(图5)。代表性的单分子定位成像方法主要有随机重建显微镜(STORM)和光激活显微镜(PALM),其中STORM使用具有光开关性质的荧光染料,而PALM使用光激活荧光蛋白[12,13]。
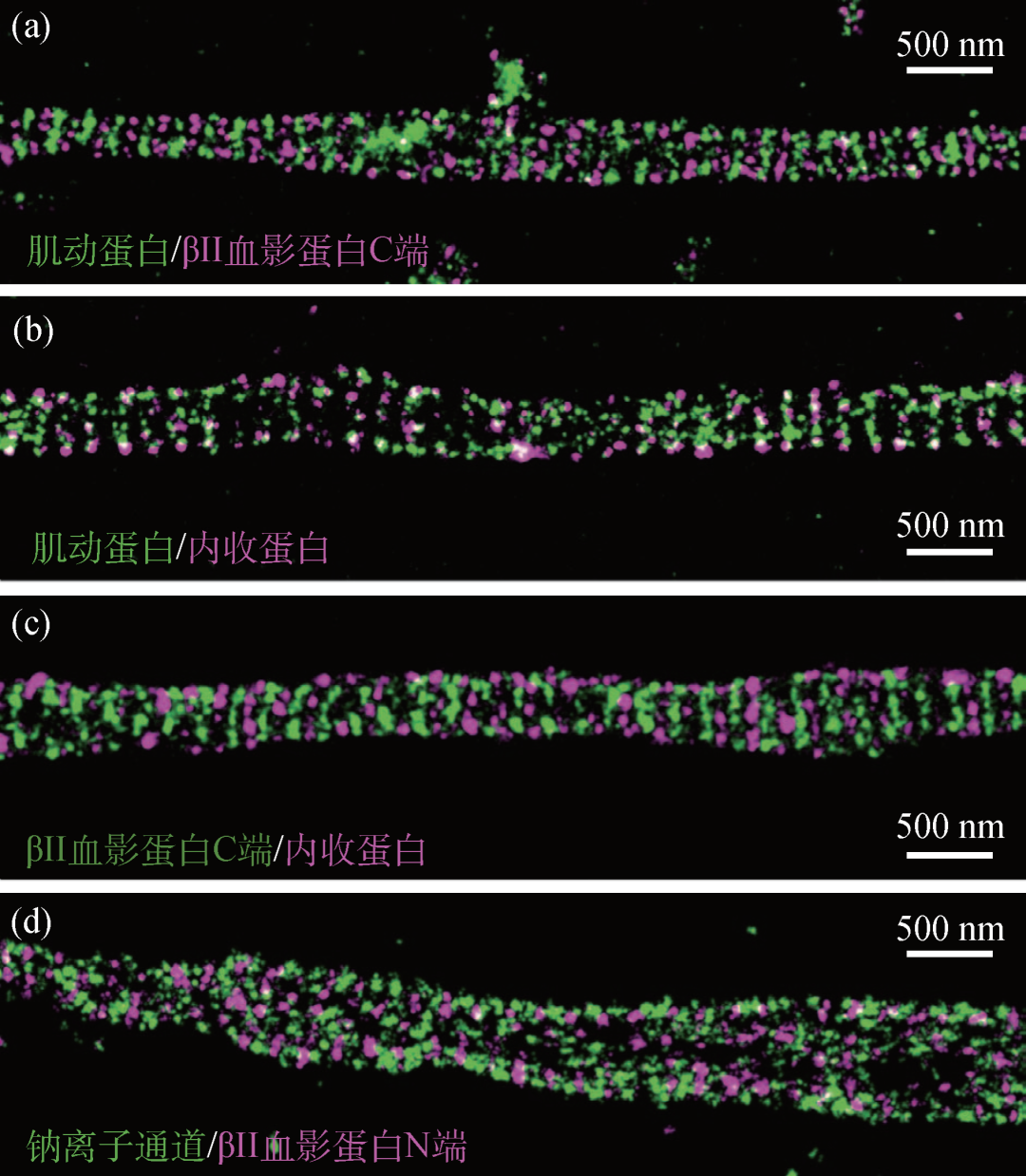
图6 SMLM技术解析神经轴突周期性结构[14]。分别对神经元轴突中肌动蛋白(图(a),(b)中的绿色通道),βII血影蛋白(图(a),(d)中的红色通道,图(c)中的绿色通道),内收蛋白(图(b),(c)中的红色通道)以及钠离子通道(图(d)中的绿色通道)的分布进行超分辨率解析,发现这些组分呈现周期性交叉排列。此前使用传统显微成像技术一直无法观察到这种结构。这一结构的解析对于轴突的形态和功能研究具有重要意义
SMLM技术把荧光显微镜的分辨率提高了一个数量级,这项技术解析了众多未知的细胞纳米结构,提升了我们对细胞的认知。例如,2013年,庄小威等人利用发明的STORM技术解析了神经轴突上肌动蛋白和离子通道的周期性排布(图6),而在此之前这种结构受限于分辨率的限制,一直未能被发现[14]。另外,2013年,科研人员使用SMLM技术对核孔复合物(nuclear pore complex,NPC)进行成像(图7),表明SMLM技术有望成为研究生物大分子机器的一种新方法[15]。因为执行生命活动的许多基本单元,在几十纳米尺度上有着复杂精细的组装结构,因此,对生命活动本质的理解需要发展更高分辨率的成像技术。近几年这个领域也得到突飞猛进的发展。其中最具代表性的是MINFLUX(minimal photon flux)[16]和重复光学选择性曝光技术(repetitive optical selective exposure,ROSE)显微镜[17,18]。
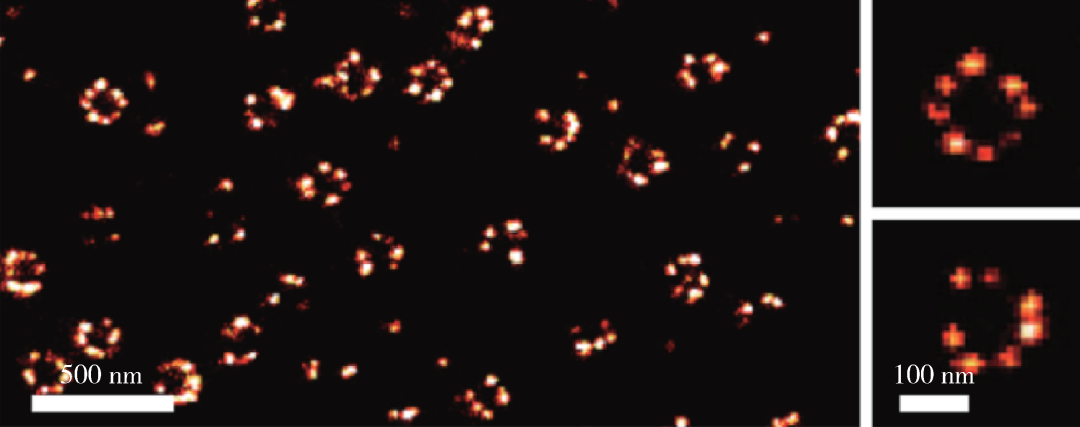
图7 SMLM技术解析核孔复合物[15]。左图为NPC成像结果,右侧两图为典型的NPC八聚体结构。通过解析核孔复合物的八聚体结构,说明SMLM技术在解析生物大分子复合物方面具有很大潜力
传统的SMLM技术使用质心拟合算法来计算单分子图像的中心,作为分子的定位信息。该方法采取二维高斯函数模型对单分子图像进行拟合,对单分子的中心位置、大小以及亮度等参数进行估计,其中位置信息将被用于后续图像重构。单分子定位显微镜的分辨率受到单分子定位精确度影响,因此通常使用单分子的定位精度来表征,它本质上是无偏估计的标准差,单分子定位显微镜的分辨率约为定位精度的2.3倍。理论上,如果忽略采样率和噪声的影响,质心拟合的定位精度可表示为[19]
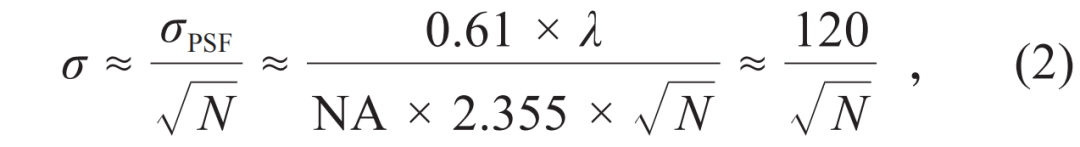
式中,σ是定位精度,σPSF是点扩散函数(PSF)用高斯函数近似拟合出来的标准差,N是单分子的光子数。由此可见,单分子定位成像的分辨率高度依赖于分子的光子数,当单分子光子数为1000时,再考虑背景光子数的影响,对应的单分子定位精度约5—10 nm。为了进一步提升单分子的定位精度,近年来该领域大部分工作集中于提高检测到的光子数,比如新荧光探针开发、抗漂白试剂、低温成像、采用双物镜系统收集等,但单分子定位的原理一直没有得到突破。
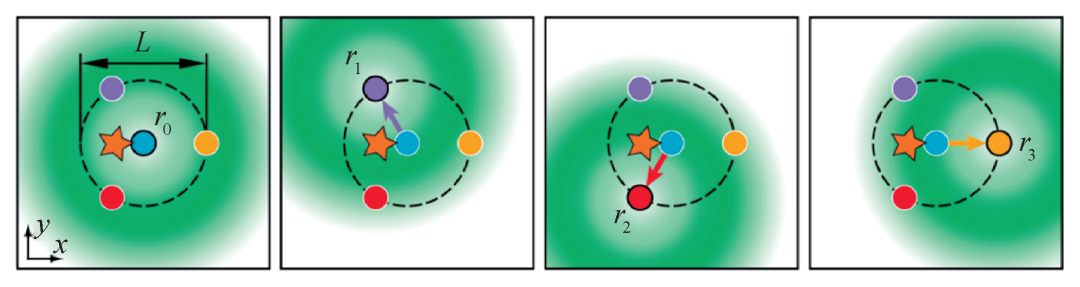
图8 MINFLUX原理图[15,16]。图中黄色五角星表示荧光分子,四个颜色圆点表示四次照明的光斑中心位置,绿色部分表示实际的空心照明光斑。通过使用空心照明光斑围绕单分子进行四次激发,实现对单分子的精确定位
2017年,诺贝尔奖获得者Stefan W. Hell提出了MINFLUX显微镜概念[16]。这个技术创造性地利用STED显微镜的类似甜甜圈(donut)的光场分布来激发STORM显微镜里所用的光控荧光探针,以保证激发光场内仅存在一个荧光分子(图8)。移动光场位置可获得不同激发光强下荧光分子的信号强度,也就是光子数,通过分析光子数与光场之间的关系,就能精确判断分子的位置。相同光子数下,可以大幅度提高定位精度和分辨率。此外,由于该技术用极少的光子数就可以获得非常高的定位精度,非常适合进行单分子追踪应用,可以提供非常高的空间、时间分辨率去进行追踪单个荧光分子。
MINFLUX技术虽然具有非常高的空间分辨率,但也存在一个缺点,即该技术利用单个甜甜圈状的光点激发荧光分子,因此同一时间只能定位或追踪一个分子,成像通量太低,数据收集所需时间较长。特别是对于较大或较致密的细胞结构来说,不适合应用该技术解析。
为了在不损失成像速度和通量的前提下提升单分子定位成像的分辨率,中国科学院生物物理研究所的团队发展了干涉单分子定位显微镜技术[17,18]。同样是利用面照明和相机高通量检测,与传统质心拟合定位方法不同的是,这项技术采用了干涉定位代替现有的单分子图像质心定位,通过利用激光干涉产生明暗相间的条纹来激发荧光分子,进一步提高了单分子的定位精度。这种单分子定位方法被命名为重复光学选择性曝光技术(ROSE)[17],其定位精度公式如下:
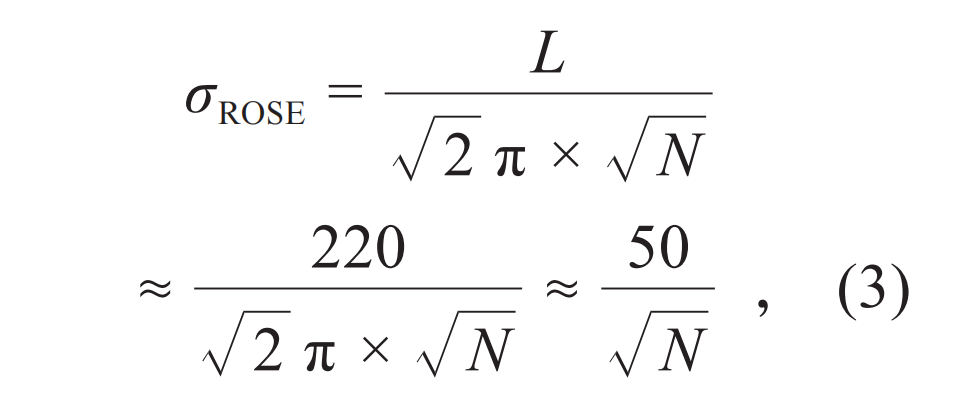
式中L是干涉条纹的周期,取决于波长和物镜的有效数值孔径,实测中能达到220 nm。在相同光子数条件下,ROSE的理论定位精度能够达到质心拟合的2.4倍。
ROSE定位原理与卫星定位类似。在卫星定位中,通过测量几颗卫星与目标的距离,即可确定目标在地球上位置。在ROSE技术中采用的干涉条纹就起到卫星的作用,3种相位间隔120°的干涉条纹被用来激发荧光分子,条纹的周期和相位都是已知的,不同条纹激发出不同强度的荧光信号,可用来确定目标分子在条纹里的相对位置。基于这个定位原理,单分子定位成像的分辨率被进一步提升到纳米级别,研制的纳米分辨率显微镜可以对细胞内微小结构的细节进行观察和分析,满足生物学研究对分辨率越来越高的需求。
横向干涉单分子定位成像[17]系统是一套二维定位系统。进行二维定位一共需要6个干涉条纹(XY方向定位需要每个方向3个相位的干涉条纹),其中X方向单分子的位置可通过对应的3个子图像保留的亮度信息获得。通过同步电光调制器和高频谐振镜,将3个干涉条纹与相机3个子区域一一对应,快速产生干涉条纹并成像(图9(a))。亮度和稳定性均较高的纳米荧光小球被用来进行系统定位的性能测试,通过对同一个小球进行多帧成像,可以方便直观地表征系统的定位精度。测试结果显示,在相同的亮度条件下,使用干涉定位能够将定位精度提高至2.4倍左右,与理论计算相符。
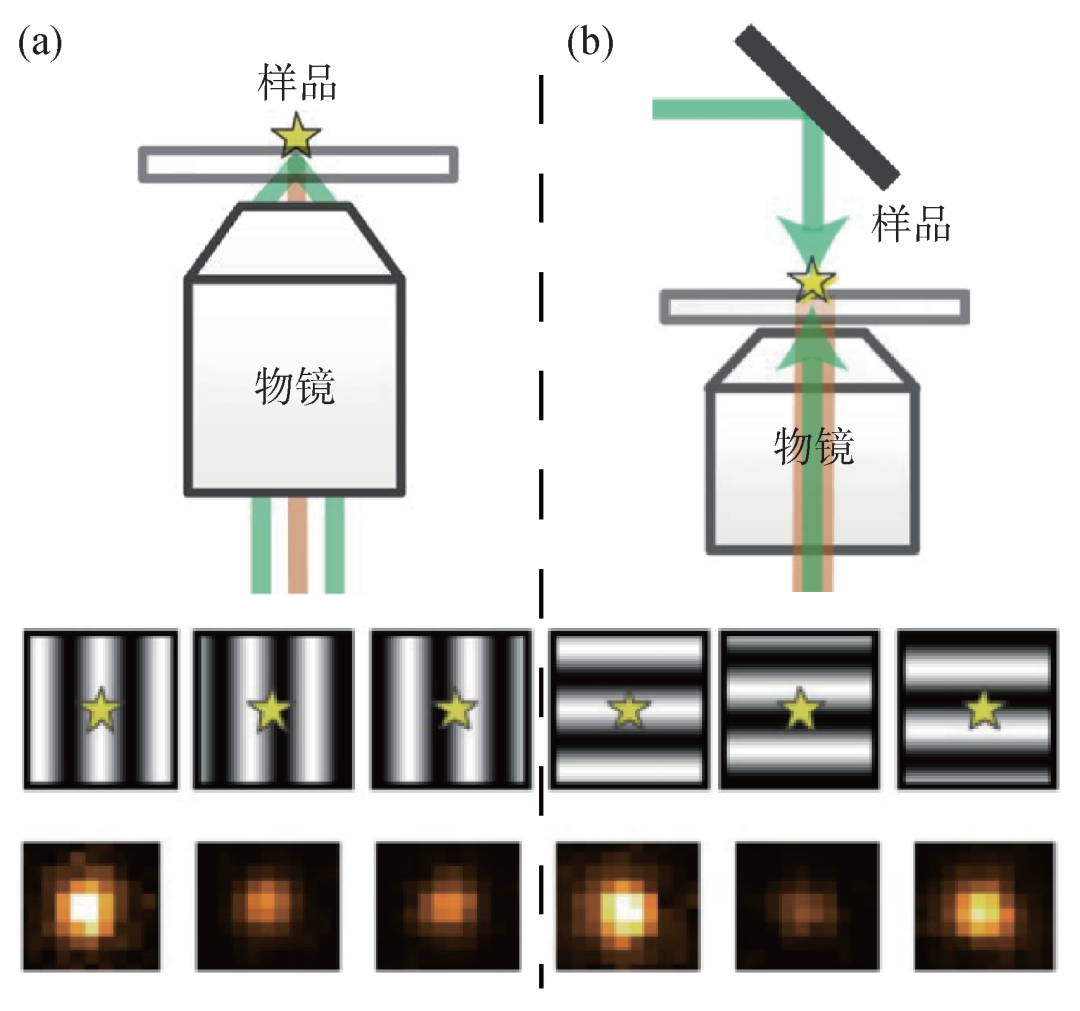
图9 (a)ROSE-XY成像技术原理图;(b)ROSE-Z成像技术原理图[17,18]。ROSE-XY成像中,使用XY方向的干涉条纹对荧光分子进行激发(左上)。ROSE-Z成像中,使用Z方向干涉条纹对荧光分子进行激发(右上)。下方两图分别表示了单分子(星形)和照明条纹(黑白图案)的相对位置,以及所对应得到的单分子图像
生物结构本身是三维的,因此轴向(Z)分辨率的提升是超分辨成像技术的重要研究方向。传统轴向定位方法主要包括柱透镜法[20]、双层成像法[21],以及点扩散函数(point spread function,PSF)工程法[22]。由于显微镜轴向分辨率本就比横向分辨率差,导致单分子定位成像中轴向定位精度比横向定位精度差2—3倍,一般为50 nm左右。
为了提高轴向定位精度,干涉单分子定位技术也被应用于轴向定位,并被命名为ROSE-Z[18]。使用非对称光路结合ROSE技术,实现了单分子轴向定位,如图9(b)所示。同柱面镜法相比,轴向定位精度提高了6—8倍,能够实现高轴向分辨率的三维超分辨成像,可以轻松解析直径仅为23 nm的微管中空结构。
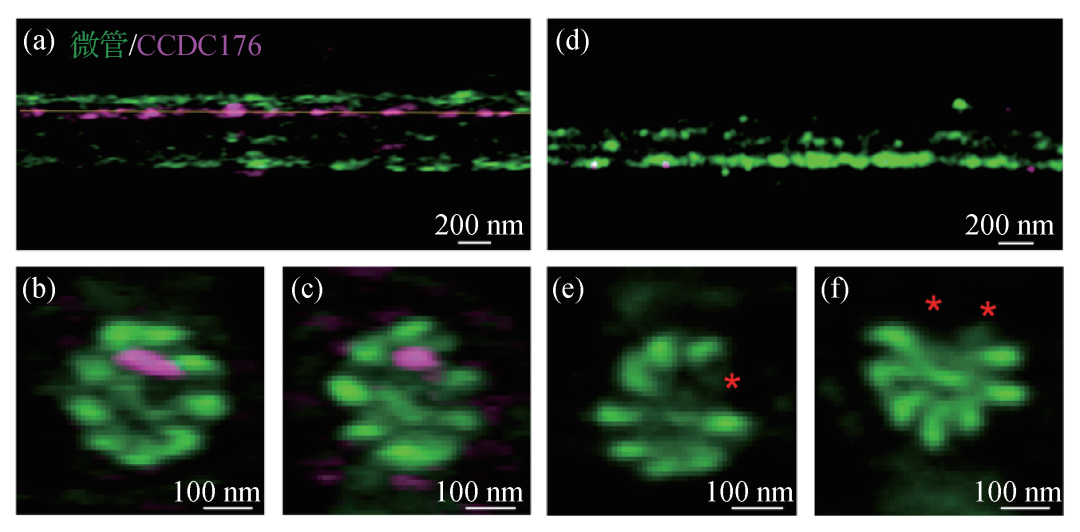
图10 ROSE-Z成像正常精子鞭毛轴丝纵截面(a)和横截面(b)、(c),及CCDC176敲除的精子鞭毛纵截面(d)和横截面(e)、(f)[23]。图中微管为绿色通道,在横截面图(b),(c)中双联微管围绕中心呈环状结构,敲除CCDC176后存在部分缺失(图(e),(f),星号表示缺失部位)。CCDC176为红色通道,位于双联管内侧非对称分布(图(a)—(c))
该技术被用于多种亚细胞结构的解析。鞭毛是精子动力的来源,在一个应用研究中,研究者发现编码定位于鞭毛的CCDC176 (coiled-coil domain-containing 176)蛋白的基因敲除的小鼠生育力会显著下降,并伴随第1和第9组的微管双联管消失[23],但其分子机制不清楚。ROSE-Z则揭示了CCDC176恰好定位在缺失双联管内侧(图10),起到锚定这两组微管双联管的作用,这个研究表明ROSE-Z在纳米结构表征和蛋白定位研究方面具有非常独特的优势。
超分辨成像技术突破了传统光学显微镜衍射极限的限制,实现了对细胞内各种精细结构的观察以及目标蛋白分子定位分布的研究。以单分子定位显微镜技术为代表的多种超分辨显微成像技术的不断发展,为揭示生命的奥秘提供了一种强有力的研究工具。
近几年发展的纳米分辨率单分子定位成像技术,与传统基于单分子图像拟合的质心定位技术不同,利用具有不同强度空间分布的光场激发荧光分子,通过分析单个荧光分子的信号强度及与光场关系来判断分子的空间位置。这一新技术的出现为生命科学研究提供了新的手段,并逐渐应用于生物大分子机器原位成像研究。如近期Ardem Patapoutian课题组使用纳米分辨率成像技术,结合定点插入非天然氨基酸和点击化学标记技术,对机械力敏感离子通道Piezo 1蛋白在细胞膜上进行原位成像。证明了该蛋白亚基末端具有高度灵活性,也是电镜无法解析该区域结构的原因,并通过成像小分子激动剂、抑制剂下的蛋白末端,获取距离信息,解释了Piezo 1蛋白构象变化的机理[24]。
单分子定位超分辨技术在光学成像领域拥有最高的空间分辨率,与光片和自适应光学等技术结合,可以实现全细胞超分辨成像;而将ROSE-XY与ROSE-Z结合的ROSE-3D技术,有望可以使不同深度的荧光分子定位精度保持在同样高的水平,实现厚样品的各向同性超分辨成像。随着越来越多的单分子成像和分析方法的出现,再结合深度学习等技术,超分辨荧光显微镜在更高时空分辨率、深层成像、活细胞成像等各方面的提升优化,将不断推动生命科学、医学等研究领域的进步。
致 谢 感谢中国科学院生物物理研究所罗世行与赵先傲在本文写作过程中给予的支持与帮助。
参考文献
[1] Huang B,Babcock H,Zhuang X. Cell,2010,143(7):1047
[2] Abbe E. Archiv für Mikroskopische Anatomie,1873,9(1):413
[3] Zernike F. Physica,1942,9(10):974
[4] Nomarski G. J. Phys. Radium,1955,16:9S
[5] Minsky M. Scanning,1988,10(4):128
[6] Huang B,Bates M,Zhuang X. Annu. Rev. Biochem.,2009,78:993
[7] Hell S W,Kroug M. Applied Physics B,1995,60(5):495
[8] Hell S W,Wichmann J. Optics Letters,1994,19(11):780

