脂溶性是药物化学中小分子的重要参数,通常用 logP 与 logD 进行表示。口服固体制剂在体内吸收主要经过以下三个阶段:3. 药物分子经胃肠道渗透进入血液系统。
对于仿制制剂开发而言,前两者是主要影响药物生物等效性的关键因素,即达到自研制剂与RLD在体内释放程度的一致性就能极大程度上保证生物等效。然而体外溶出与体内溶出无论从机理或者环境角度都存在较大的差异,生物等效性评价的最终目标是入血药物分布在自研和参比之间满足对应的比例关系,药物吸收需经不流动水层后进行生物膜表面分配进而进行跨膜渗透转运,膜水界面的药物分配比例显著影响膜上药物的附积。
膜水分配即表征药物在上述两种介质中的溶解度之比;溶解度与溶解度参数直接相关,溶解参数越大极性越大,溶解度参数符合“相似相容”原理即化合物溶解度参数与溶剂溶解度参数越接近则在该介质中溶解度越大。溶解度参数主要受三维参数影响(色散力、极性力、氢键力),研究表明生物膜脂层的溶解度参数与正辛醇溶解度参数相当接近,故而正辛醇常作为测定分配系数时模拟生物膜的一种溶剂。在药物化学和生物化学领域,理解分子的物理化学性质是至关重要的。今天,我们将深入探讨4个核心参数:LogP、LogD、pKa 和 pH,它们是评估和预测分子行为的关键指标。对于可以电离的分子,水的 pH 值会影响存在的离子数量。由于离子的特性与中性分子不同,这会影响分子的亲脂性。pH值的计算公式很简单,就不解释了,我们身体不同部位的 pH 值会影响药物的吸收和疗效。这就是为什么了解我们的分子在不同 pH 值条件下如何反应至关重要的原因。
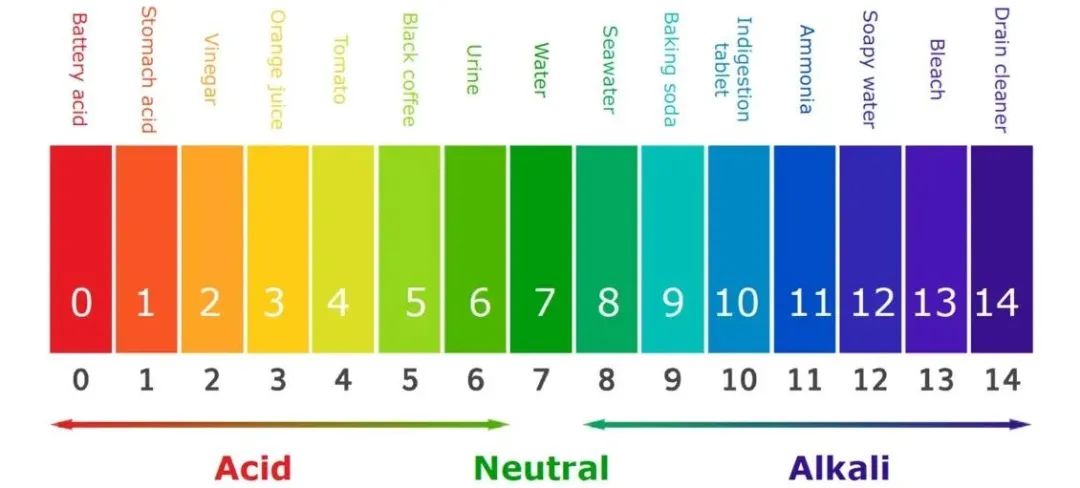
题外问题:
二、pKa
pH 是一个宏观的概念,它告诉我们溶液的总体酸碱状态,但不提供关于溶液中特定化合物的信息。与 pH 不同,pKa 是一个微观的概念,它提供了关于特定化合物在水溶液中电离倾向的信息。
Ka 称为酸解离常数,衡量酸释放氢离子的难易程度,即酸的强度,值越低,酸性越强。pKa与溶剂的pH值有关,当解离一半时,pKa=pH。
这里提一下:共轭酸是获得质子 H⁺ 的碱、共轭碱是失去质子 H⁺ 的酸。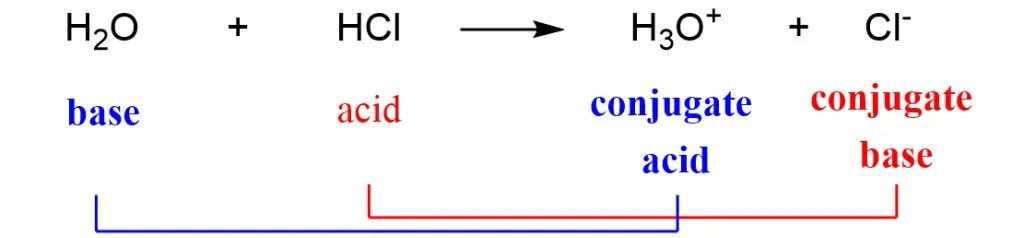
分子官能团具有特定的 pKa 值,显示了酸和碱在不同 pH 值下的电离情况:酸:当 pH值> pKa 时,化合物被电离。当 pH值< pKa 时,化合物呈中性。碱:当 pH值> pKa 时,化合物呈中性。当 pH值< pKa 时,化合物被电离。LogP :为化合物油水分配系数 P 的对数值, 指未解离的分子在非极性溶剂(一般为辛醇)和水中的分配平衡。logP 值越高,化合物的亲脂性越强。logP 值与化合物的水溶性、透膜性、体内 ADME 过程以及化合物与受体的亲和力均存在密切的关系, 在化合物透过生物膜的过程中具有关键作用.
口服药物通过被动扩散渗透时,logP值最好在 0-3,高logP化合物水溶性差,低logP化合物脂渗透性差。
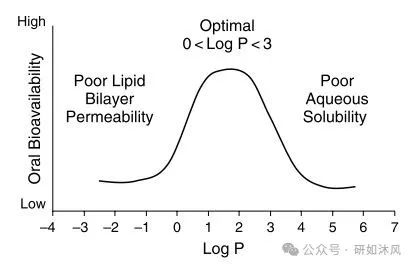
①为什么logP值最好在0-3范围是最佳的?为什么不全是亲脂性的或全是亲水性的呢?而当考虑到不同 pH 条件下化合物的存在状态不同, 引入了 log D 来描述所有存在形式的化合物(离子与分子形式)在非极性溶剂(一般为辛醇)和水的分配平衡。
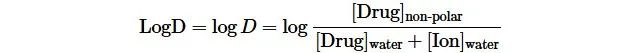
D=化合物所有解离和非解离形式在正辛醇和水中总浓度的比值。与 logP 类似,logD 的值越高,化合物的亲脂性就越强。同样,该值越低,化合物的亲水性越强,因此水溶性越好。化合物的所有电离态可以以不同的浓度存在,具体取决于生理环境的 pH 值,意味着 pH 值可以直接影响给定分子的特性,从而影响生物利用度。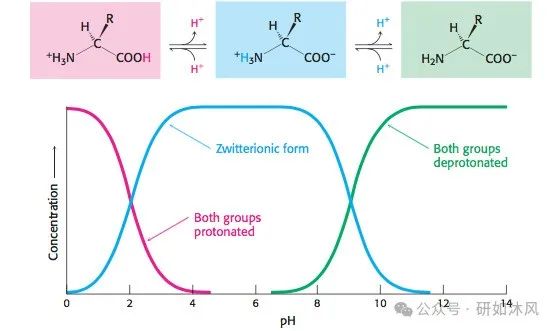
大部分药物都含有离子基团,呈碱性,可通过修饰药物分子中的酸碱基团来获得理想的pKa,从而影响药物的溶解性与渗透性,当pH=pKa时,离子组分与中性分子浓度相等。
- 对于酸性化合物:溶液pH下降,药物中性分子浓度升高,离子组分浓度减小。
- 对于碱性化合物:溶液pH下降,药物中性分子浓度减小,离子组分浓度增大
离子化的组分溶解性好,但渗透性差,高渗透性的化合物通常溶解性低。碱性化合物比酸性化合物更易于透过血脑屏障。- 酸性化合物:logD=logP-log(1+10^(pH-pKa))
- 碱性化合物:logD=logP-log(1+10^(pKa-pH))
上述结果表明,随着pH值的升高,酸性化合电离增加,离子型化合增多,即在水性介质中化和物分配增加,logD 降低;随着pH值的降低,碱性化合物电离增加,离子型化合增多,即在水性介质中化和物分配增加,logD 降低。通常采用logD(pH7.4)来表达药物在肠道环境中的表观分配系数。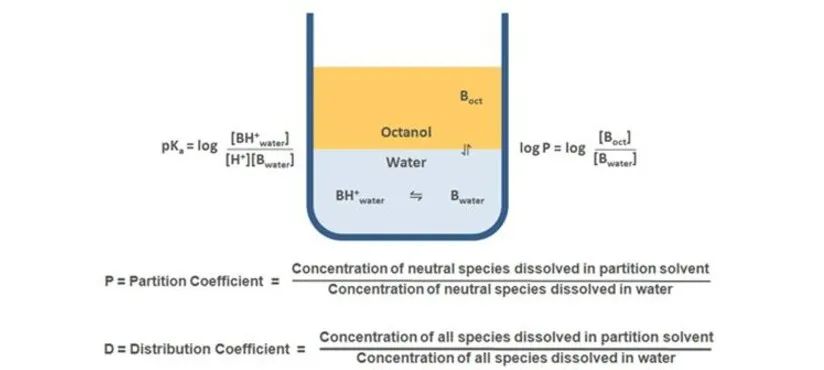
对于不可电离化合物,LogP = LogD (在整个 pH 范围内),而对于可电离化合物,LogD 则考虑了电离和非电离形式的分配,更便于实际测量,在药物代谢动力学中具有重要的意义,综合药物在体内生物膜分配情况进行评估体外溶出差异对体内吸收差异的影响有助于生物等效性的思考。对于亲脂性较强或者具有丰富膜转运蛋白化合物而言膜分配药物含量将显著影响渗透入血药物量,所以在这种情况下对体外释放趋势一致性要求较高(或均为快速溶出);对于亲水性强的化合物而言,膜分配能力较弱药物主要在水相分配体内释放差异对渗透影响较小,所以体外的溶出释放趋势一致性并不是必须的(只需满足在相当的释放即可)。Lipinski的“五法则”(Rule of Five),是评估一个化合物能否作为药物,或者一个具有药理学活性或生物学活性的化合物能否成为口服药物的经验法则。根据这一规则,成功的候选药物应具有以下特性:
其中,第三条明确指出,脂水分配系数的对数值(LogP)不大于5,这是因为过高的LogP值意味着化合物过于亲脂,可能会影响其水溶性和透膜性,从而影响药物的吸收和分布。因此,根据Lipinski的“五法则”,一个化合物若要成为成功的口服药物候选,其LogP值不应超过5。五、logP和LogD在药物研发中的应用
在药物研发中,化合物的亲脂性与其在体内的渗透性相关,下面,我们将讨论使用logD代替logP评价渗透性的意义。下图显示了口服化合物在胃肠道中可能遇到的pH环境的变化,药物经过的pH环境并不是一个恒定不变的,因此,根据不同的pH精准计算logD是非常有必要的。我们以化合物5-甲氧基-2-(1-哌啶-4-基丙基)吡啶作为例子,详细说明基于logP和logD值分别进行亲脂性判断,看看这两个参数结果对我们最终的判断有何区别。该化合物的吡啶环(4.8)和哌啶环(10.9)具有不同的pKa,因此在不同的pH值下具有不同的质子化形态。该化合物在生理pH(1-8)下几乎不存在中性形式(红色表示中性形式)。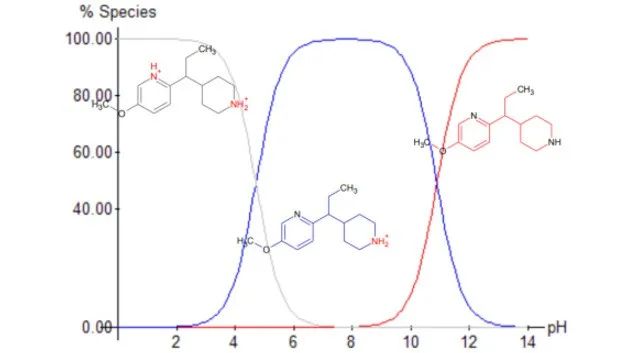
通过ACD/Labs软件计算该化合物的logP为2.66 ± 0.28,表明这个化合物的脂溶性很好。
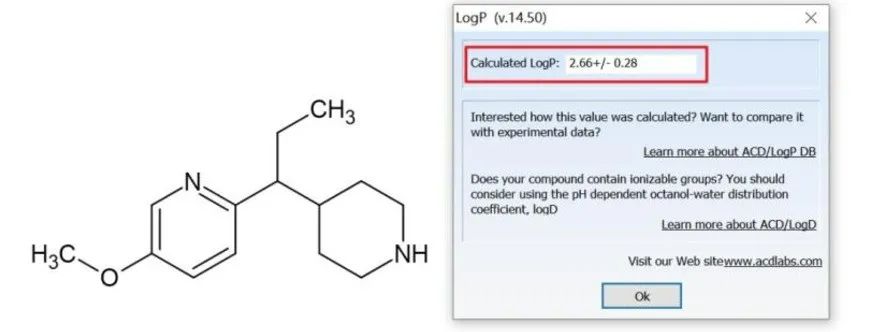
如果仅靠LogP作为依据得出的结论是,该化合物的脂溶性理想,渗透性也应该较好。然而事实并非如此,再看计算的LogD值(通过ACD/Percepta软件预测得到),如下图所示:
LogD值反映出该化合物在生理环境下,脂溶性非常低,pH小于12的环境下脂溶性都不理想。由此可推断,该化合物在体内的细胞膜渗透率是很差的。这一结论与LogP推断的结论完全相反。
以上我们介绍了来自药物研发中区分logP和logD的例子,但在其他研究领域同样适用。例如,在环境化学中,在研究受不同土壤或酸雨影响的化学物质的行为时,化合物不同电离形式的存在是与pH相关的,因此同样应重视logD的考量。
综上,LogP和LogD虽然都是反映分子亲脂性的描述符,但是LogP适合中性分子的亲脂性表征,虽然它可以作为比较总体趋势的一个非常有用的参考,但在使用时应谨慎。对于因pH而具有不同电荷状态的分子,更适合使用考虑了pH变化的LogD来描述其亲脂性。

