
Upconverting nanoparticle-containing erythrocyte-sized hemoglobin microgels that generate heat, oxygen and reactive oxygen species for suppressing hypoxic tumors
包含上转换纳米粒子红细胞大小的血红蛋白微凝胶用于产热、氧和活性氧用于抑制乏氧肿瘤
Kim Hanju; Yoon Johyun; Kim Hwang Kyung; Lee Woo Tak; Nguyen Nguyen Thi; Le Xuan Thien; Lee Eun-Hee; Lee Eun Seong; Oh Kyung Taek; Choi Han-Gon; Youn Yu Seok[J] Bioactive Materials. Volume 22 , Issue . 2023. PP 112-126 DOI:10.1016/J.BIOACTMAT.2022.09.020
主讲人:韦金昕 2024年10月20日
研究背景:
血红蛋白(Hb)是一种存在于红细胞中的天然四聚体蛋白,由1个α和2个与氧结合的β多肽亚基组成。Hb的高氧结合能力使许多纳米或微米的Hb基载氧载体(HBOC)的发展,以提供氧气作为血液替代品并模拟红细胞功能。化学修饰的Hb共轭物(交联,聚乙二醇化,聚合Hb等)和Hb包封颗粒(Hb包被/含脂质体/纳米凝胶,微球等)显示出高供氧潜力。氧合珠蛋白是一种戊二醛交联牛Hb,在欧洲和美国被批准用于兽医。此外,Hb具有更高的O2结合亲和力相较于氟碳基氧载体(FBOCs),如20%PFC修饰的氟碳人造血,并且已知在自氧化过程中通过芬顿反应生成羟基自由基(•OH)。此外,已有尝试模仿含Hb红细胞的形状、结构和功能以开发新的生物模板。同样,Hb被视为氧气治疗用途最广泛的材料之一.
光动力疗法(PDT)是一种非常有效的肿瘤治疗方法。光敏剂(PS)能够产生活性氧(ROS),例如羟基自由基和单线态氧(1O2)响应近红外(NIR)光的氧分子;这些ROS随后严重损伤肿瘤细胞。然而,由于该方法对组织氧气水平和光强度的依赖性,PDT的治疗性能在缺氧肿瘤区域中受到抑制。此外,大多数PS试剂的最大吸收波长为∼660nm,与NIR光(700-980nm)相比,该波长的光不能完全穿透深层组织。基于抗斯托克斯现象的上转换纳米粒子(UCNPs)能够从较长的激发光发射较短波长的光,已被用于提高穿透深度和照明效率。特别是吸收波长为700-980 nm的光并发出∼660 nm光的UCNP可以触发体内的光敏剂(PS)。由敏化剂和激活剂组成的镧系元素掺杂core@shell UCNP已被广泛用于最大化上转换活性。
热疗是另一种抗肿瘤疗法。已知重度热疗(>48°C,持续10分钟)可诱导肿瘤细胞快速凋亡和不可逆死亡。相比之下,39-42°C的温和热疗可增强抗肿瘤治疗药物的递送,这是因为由于血流量增加和肿瘤血管孔隙增大,血管对药物或纳米颗粒通透性提高。此外,轻度高热有助于提高实体瘤氧水平(例如,氧分压(pO2)和氧血红蛋白(HbO2)),增强化疗药物的抗肿瘤功效。因此,将热疗与主要抗肿瘤方式结合使用可以提高抗肿瘤治疗的有效性。许多传统的光热剂,如吲哚菁绿、IR780和金纳米棒,可以响应近红外激光照射控制表面温度,这取决于激光强度、照射时间和光热剂的浓度等因素。
研究内容:
作者介绍了原位可注射的多功能红细胞大小的微凝胶平台(5-6μm),其具有受控的光热和光动力活性,可响应近红外光产生热,O2以及ROS。微凝胶(Hb μGel)包括(i)血红蛋白,用于供应氧气,响应808nm激光照射而散热,(ii)白蛋白以稳定μGel体系,以及(iii)UCNP发出∼660 nm光 翻页 响应深穿透808 nm激光照射以激活光敏剂(Ce6)并产生单线态氧(1O2)。作者认为这些Hb μGels能够提高缺氧肿瘤中的O2水平,并增强光动力治疗与UCNP联合的细胞毒性作用。此外,作者认为响应NIR激光照射(808nm)的Hb放热,提高局部温度(41-42°C)而扩张肿瘤血管,或者在>48°C严重的高热可以消融恶性肿瘤。作者的制备 负载UCNP/Ce6 Hb μGel 是多功能光热和光动力注射剂,可以克服治疗乏氧肿瘤的困难。
类红细胞血红蛋白(Hb)微凝胶(μGel)系统(5-6 μm)(Hb μGels),可以(i)产生热量,(ii)供氧,(iii) 响应近红外(NIR)激光照射产生活性氧(ROS;1O2)。Hb μGels包括Hb、牛血清白蛋白(BSA)、二氢卟吩e6 (Ce6)和铒@镥上转化纳米颗粒(UCNPs;~35nm)构成,可以有效地将808nm的近红外光转换为660 nm的可见光。
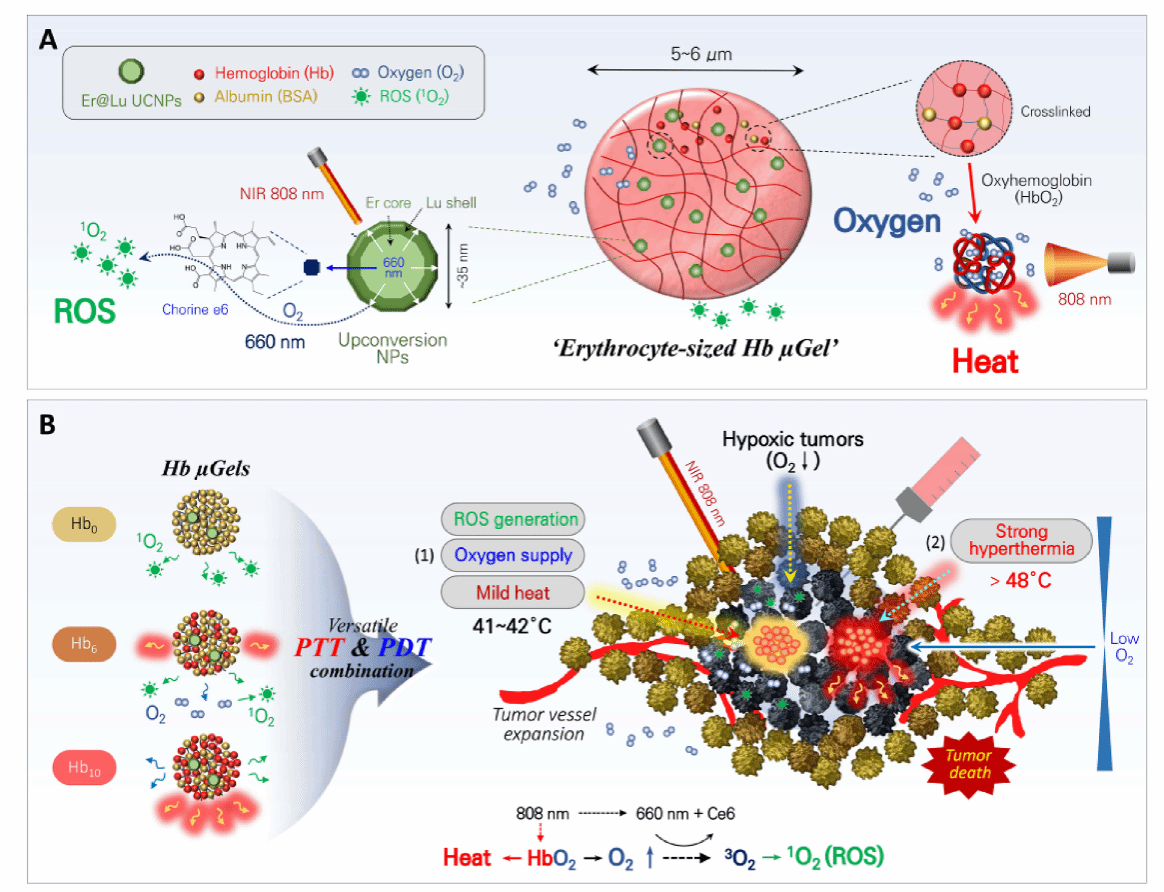
要点:
类红细胞血红蛋白(Hb)微凝胶(μGel)系统(5-6 μm)(Hb μGels),可以(i)产生热量,(ii)供氧,(iii) 响应近红外(NIR)激光照射产生活性氧(ROS;1O2)。Hb μGels包括Hb、牛血清白蛋白(BSA)、二氢卟吩e6 (Ce6)和铒@镥上转化纳米颗粒(UCNPs;~35nm)构成,可以有效地将808nm的近红外光转换为660 nm的可见光。
所讲论文主要作者、课题组、所在实验室等简介:
总结和展望:
作者成功设计并制备了尺寸为5-6μm的红细胞样血红蛋白微凝胶系统,包括Er@Lu UCNP和Ce6光敏剂,能够(i)产生热量,(ii)提供氧气,以及(iii)响应808 nm NIR激光照射产生单线态氧。作者的Hb μGel能够通过以受控方式产生(强或温和)的热量来提高周围温度,并且由于UCNP的活性和血红蛋白对氧的亲和力,可以在足够的自氧合下产生单线态氧。通过改变合成条件,Hb μGels可以设计成具有光热或光动力活性或两者兼而有之,有效抑制缺氧肿瘤球和小鼠肿瘤。由Hb μGels诱导的温和热疗在杀伤乏氧肿瘤细胞中起支持作用,因为它促进了O2的局部转运和1O2。重要的是,所有这些能力都可以通过使用单个Hb μGel系统与NIR激光照射相结合来实现。综上所述,作者的结果验证了血红蛋白微凝胶可以作为局部注射微凝胶平台的原型用于治疗乏氧肿瘤。

