1. 巨噬细胞的基础功能
巨噬细胞是固有免疫系统中的吞噬细胞,能够识别、吞噬并消化外来病原体,如细菌、病毒等。它们同时在清除坏死细胞、免疫调节和维持组织稳态中发挥重要作用。巨噬细胞根据其在不同免疫环境中的激活情况,可分化为两种主要亚型:M1型(经典激活型)和M2型(替代激活型)。这两类巨噬细胞在其表面标志物、功能、分泌的细胞因子以及对不同疾病(尤其是肿瘤)中的作用各有不同。
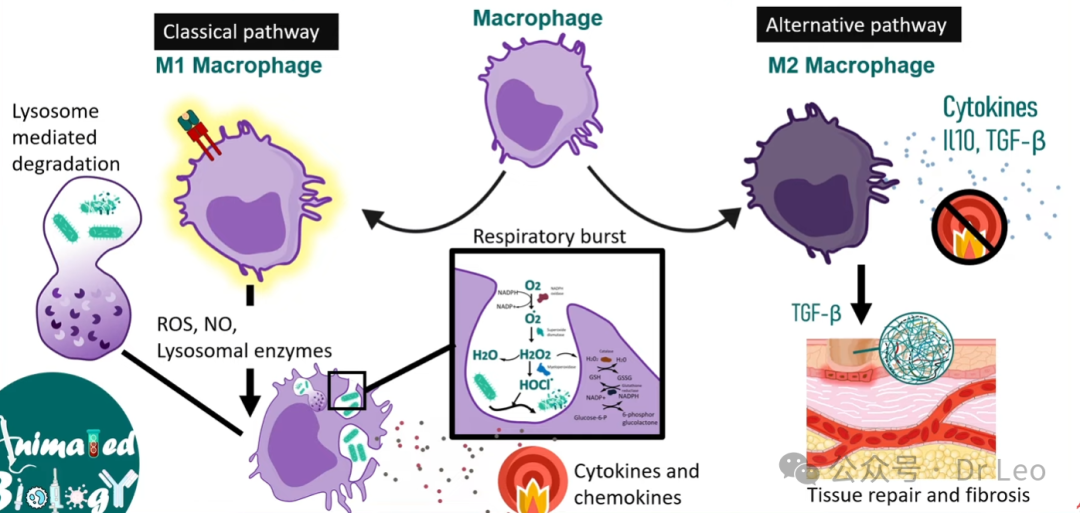
2. M1 巨噬细胞的特性与功能
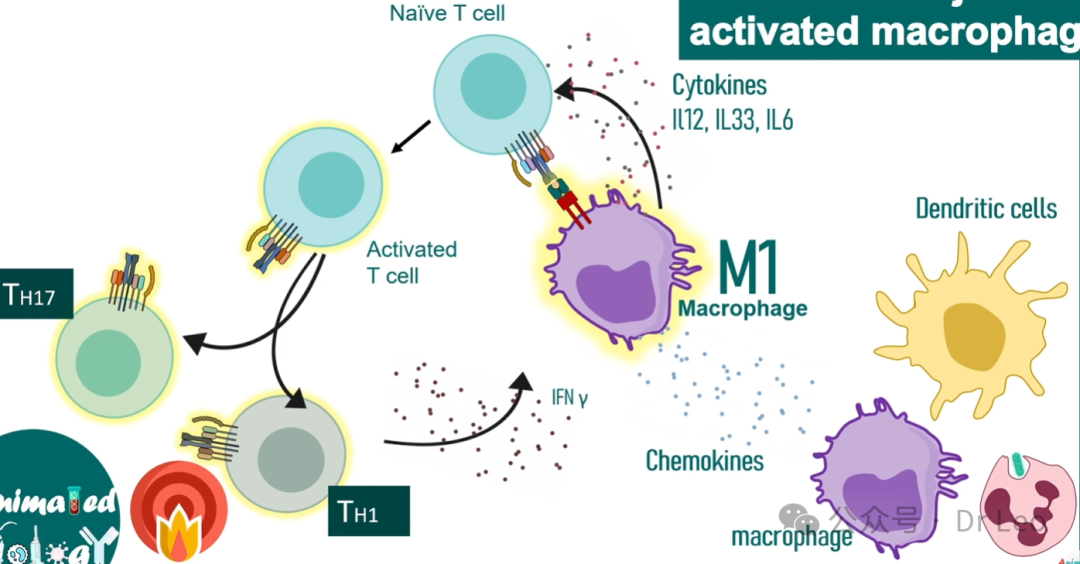
功能概述:M1 巨噬细胞通常通过经典激活途径(Classical Activation Pathway)被诱导,主要功能是启动并维持促炎性反应。它们通过分泌大量促炎性细胞因子,清除感染病原体,同时促进Th1和Th17细胞的分化,进一步加强免疫反应。激活途径:M1 巨噬细胞由干扰素-γ(IFN-γ)、脂多糖(LPS)等促炎性信号激活,属于经典激活途径。这些信号常来源于感染、组织损伤或免疫应答中的特定细胞,如活化的T细胞和NK细胞。表面标志物:M1 巨噬细胞表面高表达CD80、CD86和MHC II类分子,这些标志物有助于它们向T细胞呈递抗原,并进一步增强促炎免疫反应。分泌的细胞因子:M1 巨噬细胞主要分泌促炎性细胞因子,如IL-1、IL-6、IL-12、IL-23、TNF-α等,增强局部的炎症反应和病原体清除能力。此外,M1细胞还通过分泌趋化因子,吸引其他免疫细胞(如中性粒细胞、树突状细胞)至感染部位。
生物学功能:
病原体杀伤:通过氧化应激(呼吸爆发,Respiratory Burst)生成活性氧(ROS)和活性氮(RNS),直接杀灭病原体。
促炎反应:通过分泌大量促炎性细胞因子,维持并加剧局部炎症反应。
组织损伤:虽然M1巨噬细胞的功能在短期内有助于清除感染,但其长期激活可能导致慢性炎症和组织损伤,尤其是在一些自身免疫性疾病中。
3. M2 巨噬细胞的特性与功能
功能概述:M2 巨噬细胞通过替代激活途径(Alternative Activation Pathway)被诱导,主要参与抗炎反应、组织修复和纤维化等过程。它们在抑制炎症反应、促进伤口愈合和调节免疫平衡中发挥重要作用。激活途径:M2 巨噬细胞由抗炎性细胞因子(如IL-4、IL-13、IL-10)激活,属于替代性激活途径。这种激活通常发生在无感染或炎症的情况下,或在免疫反应的后期,用于限制炎症反应、促进组织修复。表面标志物:M2 巨噬细胞主要表达CD163和CD206(甘露糖受体),这些标志物与吞噬细胞清除损伤组织和促进愈合相关。分泌的细胞因子:M2 巨噬细胞分泌大量抗炎性细胞因子,如IL-10和TGF-β(转化生长因子-β),这些因子在减少炎症反应和促进组织修复方面发挥重要作用。
生物学功能:
抗炎作用:通过分泌IL-10等抗炎因子,抑制M1巨噬细胞和其他促炎性细胞的活性,从而缓解炎症。
组织修复与纤维化:M2 巨噬细胞通过分泌TGF-β等因子,促进伤口愈合和组织重塑,尤其在慢性伤口愈合和纤维化疾病中发挥关键作用。
免疫调节:M2 巨噬细胞通过抑制过度的免疫反应,维持免疫稳态,防止因免疫反应过度而造成的损伤。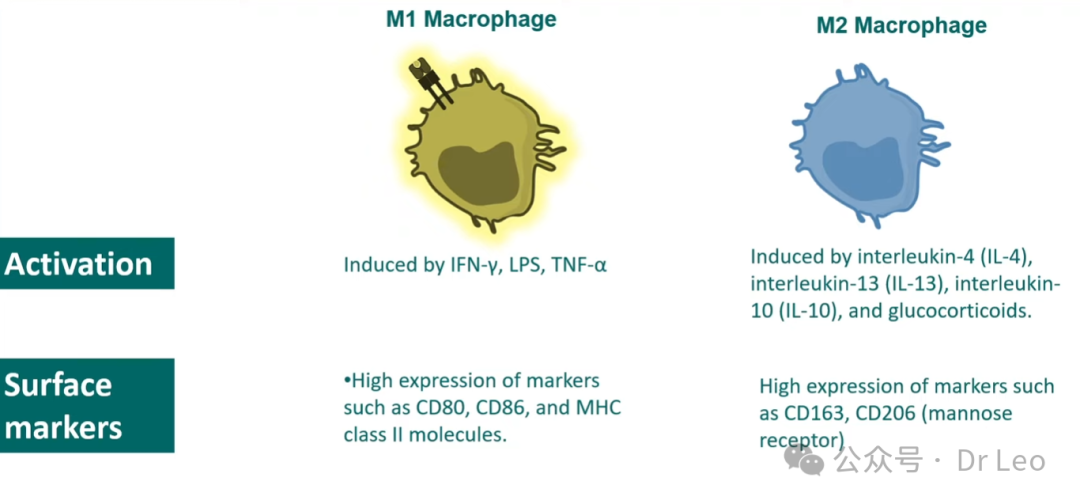
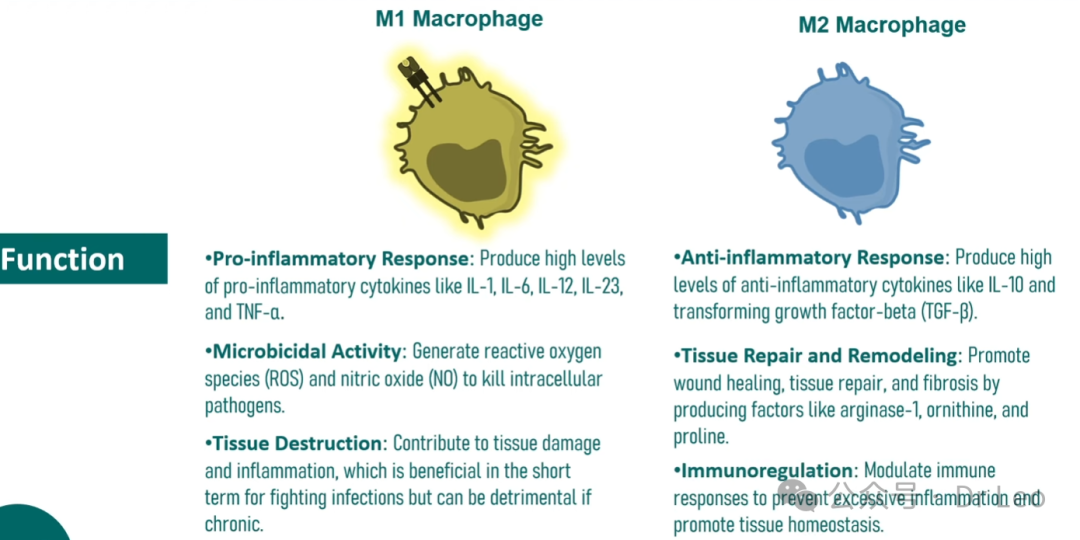
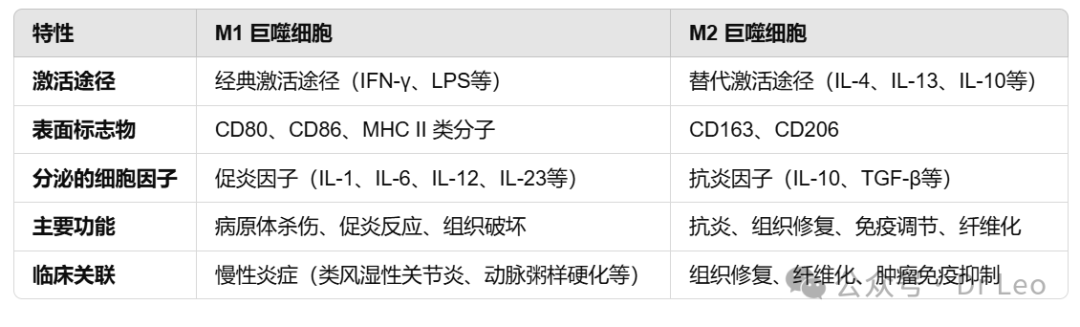
4. M1 与 M2 巨噬细胞的差异对比
5. M1 与 M2 巨噬细胞在肿瘤中的作用
肿瘤微环境中的M1和M2巨噬细胞巨噬细胞在肿瘤微环境(Tumor Microenvironment, TME)中扮演了复杂且关键的角色,通常称为肿瘤相关巨噬细胞(TAM, Tumor-Associated Macrophages)。TAM 可以表现出M1或M2特性,但大多数TAM倾向于M2型表型,这有助于肿瘤的生长和进展。
- M1 巨噬细胞在肿瘤中的作用:M1 巨噬细胞具有抗肿瘤效应。它们通过分泌促炎性细胞因子(如IL-12、TNF-α)以及通过直接杀伤机制(ROS和RNS)抑制肿瘤细胞的增殖和存活。此外,M1 巨噬细胞可以激活T细胞,进一步增强抗肿瘤免疫反应。
- 抗肿瘤效应:M1 巨噬细胞通过促进Th1免疫反应,抑制肿瘤的生长,并有助于清除早期肿瘤细胞。
- M2 巨噬细胞在肿瘤中的作用:相比之下,M2 巨噬细胞在肿瘤中具有促肿瘤效应。M2 型TAM通过分泌抗炎因子(如IL-10、TGF-β)抑制抗肿瘤免疫反应,创造有利于肿瘤生长的免疫抑制微环境。此外,M2 巨噬细胞还促进血管生成、肿瘤细胞迁移和转移。
- 促肿瘤效应:M2 型TAM通过促进肿瘤血管生成、支持肿瘤细胞的侵袭和转移,并抑制抗肿瘤免疫反应,使得肿瘤得以逃避免疫监视。
- 免疫逃逸:M2 TAM 通过减少促炎细胞因子的释放和抑制CD8+ T细胞的活性,帮助肿瘤细胞逃避免疫系统的攻击。
M1/M2 平衡与肿瘤治疗的潜力在肿瘤治疗中,调控M1/M2平衡是一种有潜力的策略。促进M1 巨噬细胞的抗肿瘤活性或抑制M2 巨噬细胞的促肿瘤功能可能成为新型免疫治疗的方向。比如,一些研究正在探索如何通过靶向TAM中的M2型巨噬细胞,重新编程其为M1型,从而增强肿瘤免疫治疗的效果。
6. 临床相关性
M1 巨噬细胞:在慢性炎症性疾病中,M1巨噬细胞往往是导致组织损伤和慢性炎症的重要因素。它们在类风湿性关节炎、动脉粥样硬化和炎症性肠病等多种疾病中起关键作用。
M2 巨噬细胞:M2巨噬细胞在纤维化疾病、伤口愈合中扮演修复和抗炎角色。然而,过度的M2活性可能导致组织纤维化,同时在肿瘤进展中也发挥负面作用。
参考文献
Mantovani, A., Sica, A., Sozzani, S., Allavena, P., Vecchi, A., & Locati, M. (2004). The chemokine system in diverse forms of macrophage activation and polarization. Trends in Immunology, 25(12), 677-686.Biswas, S. K., & Mantovani, A. (2010). Macrophage plasticity and interaction with lymphocyte subsets: cancer as a paradigm. Nature Immunology, 11(10), 889-896.Murray, P. J., & Wynn, T. A. (2011). Protective and pathogenic functions of macrophage subsets. Nature Reviews Immunology, 11(11), 723-737.Sica, A., & Mantovani, A. (2012). Macrophage plasticity and polarization: in vivo veritas. The Journal of Clinical Investigation, 122(3), 787-795.Noy, R., & Pollard, J. W. (2014). Tumor-associated macrophages: from mechanisms to therapy. Immunity, 41(1), 49-61.Qian, B. Z., & Pollard, J. W. (2010). Macrophage diversity enhances tumor progression and metastasis. Cell, 141(1), 39-51.Mills, C. D. (2012). M1 and M2 macrophages: Oracles of health and disease. Critical Reviews in Immunology, 32(6), 463-488.Locati, M., Curtale, G., & Mantovani, A. (2020). Diversity, mechanisms, and significance of macrophage plasticity. Annual Review of Pathology, 15, 123-147.Ovais, M., Guo, M., Chen, C., Zong, J., & Shi, J. (2021). Engineered M1 macrophage membrane‐camouflaged gold nanocages for targeted photothermal therapy and enhanced anti‐tumor immunity in a mouse melanoma model. Advanced Functional Materials, 31(12), 2008259.Jayasingam, S. D., Citartan, M., Thang, T. H., Mat Zin, A. A., Ang, K. C., & Ch’ng, E. S. (2019). Evaluating the polarization of tumor-associated macrophages into M1 and M2 phenotypes in human cancer tissue: technicalities and challenges in immunohistochemistry. Cancers, 11(12), 1860.

