2025年1月23日,急救与创伤教育部重点实验室于法标教授团队与合作者在国际高水平期刊《Angewandte Chemie International Edition》(德国应用化学)上发表了题为“Valence State Hydrogen Channel Enhances Sustained and Controllable Electrocatalytic Hydrogen Evolution in Diabetic Skin Wound Healing”(动态氢调控纳米通道智能驱动氢释放新策略实现糖尿病创面高效修复)的研究成果。
糖尿病由于血糖控制不佳和免疫系统抑制,显著增加了发生严重健康问题的风险,包括长期的皮肤炎症和伤口愈合延迟。虽然传统的氢气(H2)疗法在一定程度上有效,但其在皮肤上的实时可控释放能力有限。为此,本研究提出了一种新策略,通过中性条件下的电催化释放氢气,促进糖尿病小鼠和兔子伤口愈合。该策略将中性单金属电催化氢价态通道引入磷化钴(CoP)中,显著提高了CoP催化过程中*H活性物种的形成和转移,从而有效提升了中性电催化H2析出的性能。基于这一优异的催化性能,结合便捷的电解平台、持续的电解质供应和丝网印刷技术(FGSP),开发了便捷式柔性电催化器件。该器件能够实现可控的氢气释放,显著加速糖尿病小鼠和兔的伤口愈合。所设计的柔性电极具有尺寸可调、基材可互换和较强的材料适应性,能够满足临床和基础研究的多样化需求,展示了在临床医学中的巨大应用潜力。

糖尿病是心血管疾病、肾脏疾病、失明和截肢等严重健康问题的主要危险因素。血糖控制不佳、免疫系统受损、高糖环境等因素会延长糖尿病患者的皮肤炎症和伤口愈合时间。因此,设计有效的快速抗炎治疗策略,已成为保护糖尿病患者皮肤健康的重要研究方向。由于氢气具有很强的抗氧化性,能够有效中和体内的活性氧/氮物种,从而减轻氧化应激和炎症。有效调节氢气的持续释放,对于获得最佳的炎症治疗效果至关重要。为实现这一目标,氢气必须以最佳方式在活体皮肤上释放,以满足定制化的治疗需求。因此,设计和开发一种定制的氢气释放策略以实现向糖尿病皮肤伤口区域精确供应氢气,是当前面临的研究挑战。
电催化技术通过调节电压和时间,可以促进氢气(H₂)的连续释放,满足定制化的需求。然而,由于催化剂活性较低、生物相容性差,以及现有催化剂无法适应活体皮肤和电解质持续供应的挑战,这一策略在皮肤炎症治疗中的应用受到限制。为了解决这些问题,磷化钴(CoP)电极材料因其优异的生物相容性,主要用于碱性和酸性环境下的氢气电催化产生。然而,在中性条件下,通常需要通过引入贵金属(如Pt和Au)或其他金属材料来提高CoP的催化活性,但单一金属的本征催化活性较低。因此,需要开发新的机制,以提升中性条件下单一金属的析氢反应(HER)性能。此外,柔性电极具有重量轻、便于携带的优点,能够贴合曲面,并使催化剂更好地粘附在活体皮肤上。其商业设计有助于电解液的流动,并通过防水胶带和医用棉有效防止电解液泄漏。因此,结合便捷的电解平台、高性能催化剂和柔性电极的有效集成,能够有效解决上述挑战,具有广阔的应用前景。为此,通过利用一种新的价态氢通道机制,CoP 催化剂在中性条件下的析氢反应性能得到了显著提高。基于这种催化剂,开发了一种氢释放可控的柔性装置,有效加速糖尿病伤口的愈合。
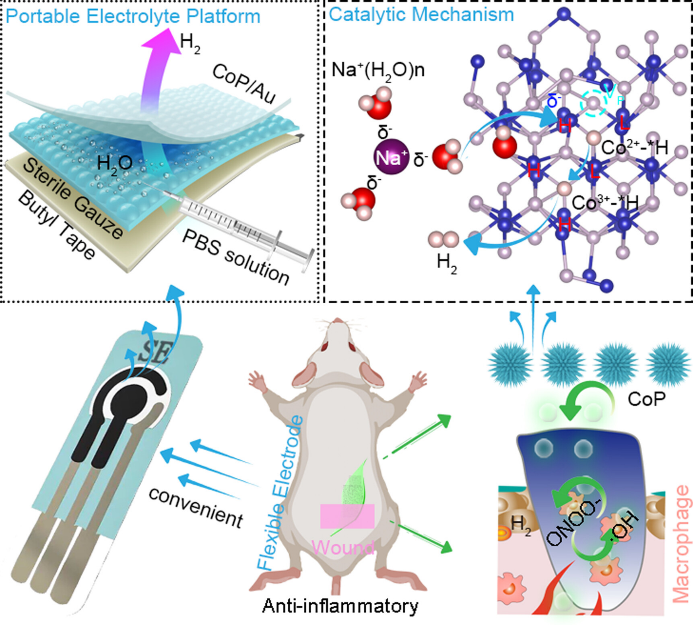
图1:CoP/FGSP材料通过实时可控氢气的生成促进活体伤口愈合应用概念图。
具有刚性基材(Ti 箔)的 CoP/Ti 电极不适合直接应用于涉及生物系统的研究,因此,该电极被转移到 FGSP 上。CoP/FGSP 可用作三电极或双电极系统,并且CoP/FGSP在不同弯曲半径(0.5-2.5 cm)和弯曲周期内表现出高电位和峰值电流的可重复性,表明出色的弯曲和电化学稳定性。在通过I-T方法使用CoP/Ti或者CoP/FGSP电极的实时制H2过程中,也没有观察到明显的细胞死亡,这表明其具有良好的生物相容性。CoP/FGSP电极通过实时可控的产生H2可以选择性地清除ROS/RNS,确保正常的细胞内信号调节,达到一定的抗炎抗氧化作用。
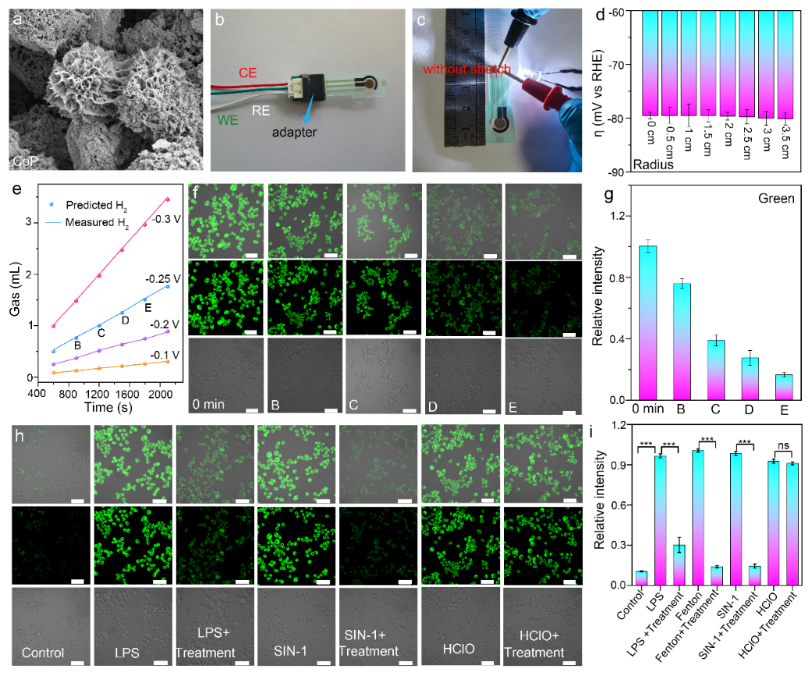
图2:CoP/FGSP在细胞水平上实时可控H2的产生。
此外,CoP/FGSP实现了在活体水平上的应用,尤其是在不同体型和伤口尺寸的活体模型中。相比之下,未经治疗的糖尿病小鼠及兔子表现出相对较低的伤口愈合率,而治疗组则表现出更快的结痂及愈合效率。重要的是,可根据不同尺寸、种类和伤口模型的要求定制不同尺寸的柔性电极 (CoP/FGSP),使其适应不同的实验条件和临床场景。这些电极对小型动物和大型哺乳动物模型的灵活性和适应性表明这些电极具有广泛的应用潜力。
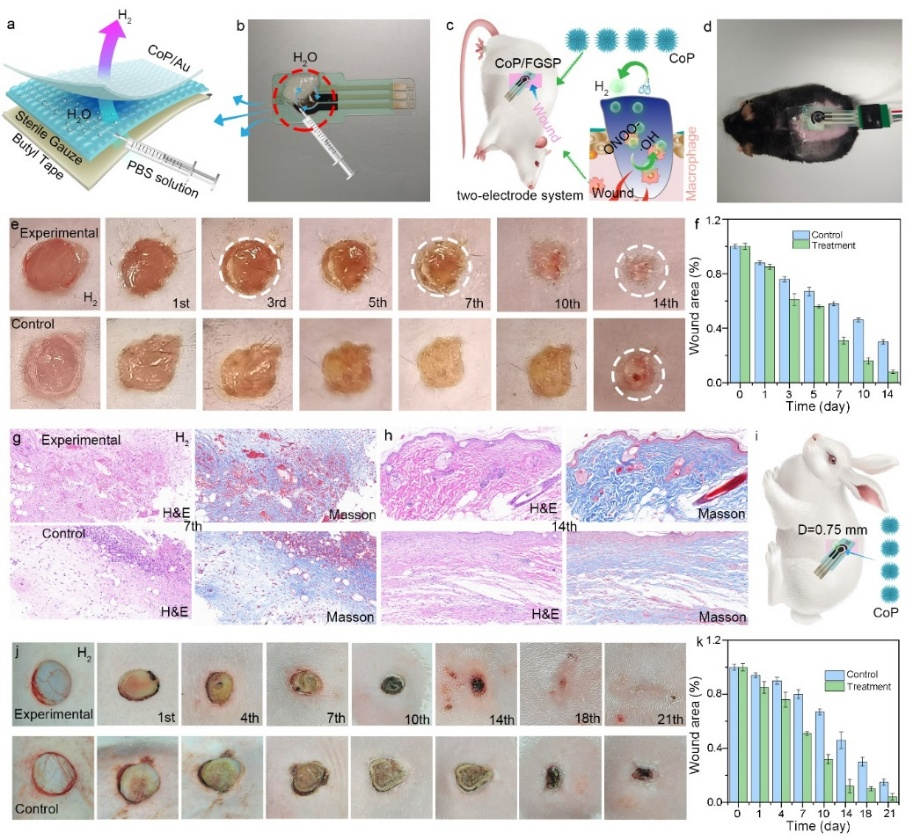
图3:构建的便携式电解质平台通过H2疗法促进糖尿病伤口的愈合。
本文提出了一种新型电催化H2释放策略,可在糖尿病小鼠伤口愈合过程中实时、可控地释放H2。该策略利用具有高电负性的 VP-CoP,促进了阳离子水簇的吸附和H活性物种(*H)的形成。由不同价位的Co活性位点构建的*H转移通道可实现 *H的高效转移和H2气体的生成,从而实现高效的H2析出。为了有效地将这一策略应用于小鼠皮肤的抗炎治疗,采用催化油墨旋涂技术将 CoP 材料与柔性电极整合在一起,重点探索了电压、时间、H2 生成效率和细胞水平炎症清除之间的内在关系。此外,便捷的电解平台还为皮肤上提供了一种实时可控的H2气体输送解决方案。CoP/FGSP首次用于改善糖尿病皮肤伤口模型的愈合率,显著加速了伤口愈合并减少了炎症。
该研究论文以海南医科大学为第一单位,第一作者为我校青年教师罗贤柱,通讯作者为海南医科大学于法标教授、北京协和医院罗攀医生和上海交通大学曹红帅教授。该研究获得了国家自然科学基金项目,中国医学科学院医学创新基金的支持。
原文链接:https://doi.org/10.1002/anie.202422091
