2024年11月8日,海南医科大学急创学院的于法标教授课题组在国际高水平期刊《Angewandte Chemie International Edition》上发表了题为“Metabolic Acidity/H2O2 Dual-Cascade-Activatable Molecular Imaging Platform Toward Metastatic Breast Tumor Malignancy”的研究论文。该论文报道了一种可被肿瘤相关H2O2和微酸性环境协同激活的近红外二区影像探针HN-PBA,并用于高对比度肿瘤成像及荧光引导手术导航的研究。与传统的“始终开启”探针及单一H2O2激活探针相比,这种双重响应机制可减少假阳性信号干扰,有助于更准确地识别肿瘤并切除原发性和转移性肿瘤。更为重要是,论文中报道的探针能够有效检测直径 ≤ 0.7 mm的肺转移灶,并在临床乳腺癌标本中展示了精确区分病变及正常组织的能力。这一双重刺激响应策略可能为未来诊断探针的设计做出重大贡献。

研究背景:肿瘤治疗不彻底导致的转移扩散是造成癌症高死亡率的主要原因。三阴性乳腺癌(TNBC)的侵袭性和转移性使其成为对人类健康和生命威胁最大的亚型肿瘤。在各种癌症治疗方法中,保乳手术(BCS)是一种常见的治疗策略,有时甚至是唯一的选择。在保乳手术中,CT、MRI或PET-CT等术前成像工具可用于定位和确定肿瘤大小。外科医生随后依据经验和视觉线索对肿瘤进行干预。尽管已取得了一些进展,肉眼在检测小肿瘤灶及准确区分肿瘤与正常组织边界等方面仍存在局限性。此外,术中苏木精和伊红(H&E)冰冻切片染色是评估手术边缘的黄金标准。然而,该方法操作复杂,过程漫长(超过50分钟),无法在手术过程中及时反馈治疗结果。鉴于精确的肿瘤边缘评估和全面的病灶切除对防止局部复发至关重要,而局部复发往往需要额外的手术干预,因此迫切需要开发专门针对TNBC术中应用的高效治疗策略。
近年来,荧光引导手术导航在识别肿瘤边界及切除病灶等应用上受到广泛的关注。近红外二区(NIR-II,1,000-1,700 nm)成像具有更深的组织穿透性和前所未有的时空分辨率,从而提高了肿瘤手术的准确性。基于近红外荧光的分子影像试剂在临床肿瘤研究和肿瘤学应用中均有报道,可进一步分为以下两类:i) “始终开启 ”成像探针,如吲哚菁绿(ICG)和亚甲基蓝(MB)。遗憾的是,这些探针通常在肿瘤中停留时间较短,且迅速从体内代谢,这给长期成像引导切除术带来了巨大挑战。此外,这些临床批准的探针以 “常亮 ”模式工作,它们只是在肿瘤区域积聚,而无法被肿瘤内标志物特异性激活,导致检测特异性低,对病理种类的反应不理想;ii) 生物标志物可激活成像探针,此类探针仅在肿瘤相关基质存在时才可特异性发射信号,提供实时生物信息和高信噪比(SNR)。然而肿瘤区域的一些异常表达物种在一定程度上也可能存在于正常组织中。此外,具有类似肿瘤特征的非癌症组织或器官也可能在肿瘤发生之前触发非特异性探针激活。可能导致 “假阳性”,影响肿瘤诊断的准确性。因此,使用单因素激活标准无法提供足够的对比度来有效区分肿瘤边缘和正常边缘。相比之下,多靶点级联反应探针策略已成为生物医学领域一种可靠且前景广阔的方法。这种策略可以在多种生物标记物存在的情况下选择性地激发探针荧光信号,大大减少来自非肿瘤区域的干扰信号,提高肿瘤定位的精确度。
为此本文作者构建了一种可被肿瘤相关H2O2和微酸性环境协同激活的近红外二区影像探针HN-PBA,并用于高对比度肿瘤成像及荧光引导手术导航的研究。
一:本研究中探针设计、双激活响应及活体和临床样本的成像应用概念图
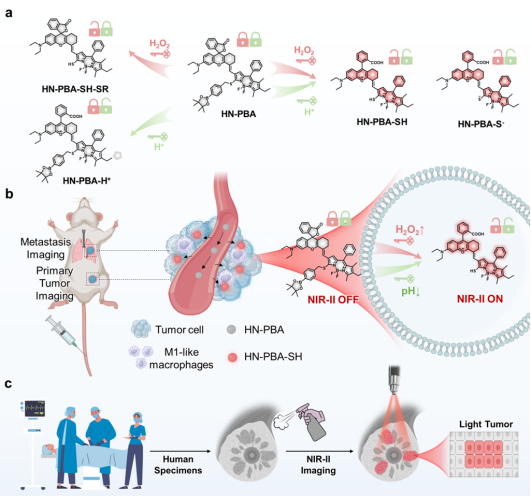
本研究的双激活响应概念图及活体和临床样本的成像应用
二:探针水溶液多靶标级联响应探究
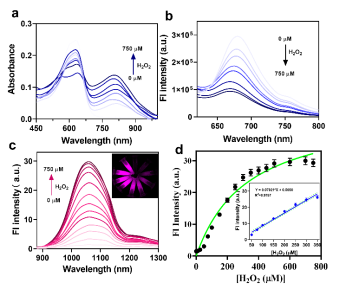
探针只有在弱酸性环境中才可对H2O2有较好响应, 并激活1060 nm 处的近红外二区荧光.
三: 小鼠皮下多肿瘤成像
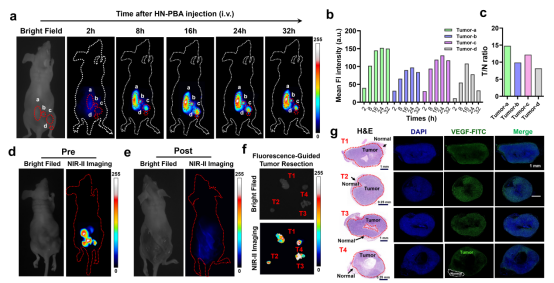
探针能以超过10倍的成像对比度区分肿瘤与正常组织; 通过特异性的近红外二区荧光引导,切除后的肿瘤残留的阴性边界直径约为0.25 mm.
四: 小鼠肺转移成像研究
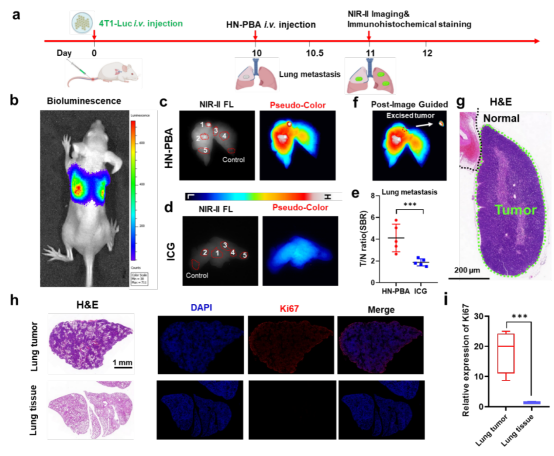
五:临床样本成像
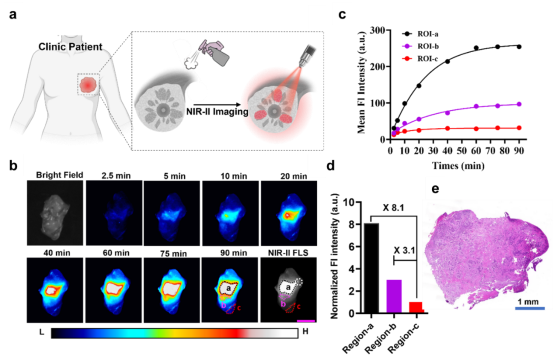
经过原位喷涂的方法,新鲜切除的临床乳腺肿瘤样本可在60 min 内点亮病灶部位。
创新点和意义:本论文以肿瘤酸性环境及过表达的H2O2 为研究对象,构建了多靶标级联激活NIR-II 分子探针用于肿瘤成像研究。该探针的 “双锁匙 ”设计最大程度地减少了非特异性激活和潜在的假阳性。皮下多发性微小肿瘤模型的病理数据表明探针可以精确识别并切除直径小至 0.25 毫米的手术阴性边缘肿瘤。得益于高分辨率和高特异性 NIR-II 荧光成像,探针可以实现原位和转移的乳腺病灶精准定位且直径约 0.7 毫米的微小肺转移灶也可轻松切除。同时,在临床癌症标本中,该探针也能有效划定肉眼难以区分的病灶和边界。我们希望这种多刺激协同激活策略能促进可靠的荧光诊断试剂的开发,用于临床术前肿瘤诊断和术中导航。
该研究论文第一作者是海南医科大学青年教师窦昆,通讯作者是海南医科大学青年教师窦昆、于法标教授和韩国高丽大学Jong Seung Kim教授。研究获得了国家自然科学基金青年项目,海南省“南海新星”科技创新人才,海南省重点研发等项目的支持。
原文链接: https://doi.org/10.1002/anie.202419191
完整作者信息:Kun Dou*†[a], Jiao Lu†[a], Yanlong Xing[a], Rui Wang[a], Miae Won[b],[c],[d], Jungryun Kim[b], Fabiao Yu*[a] and Jong Seung Kim*[b],[c]
Key Laboratory of Haikou Trauma, Key Laboratory of Hainan Trauma and Disaster Rescue, Key Laboratory of Emergency and Trauma, Ministry of Education, The First Affiliated Hospital of Hainan Medical University Hainan Medical University, Haikou 571199, China
