11月22日,我校药学院教师胡宇斯联合南开大学化学学院团队,在国际权威学术期刊《Journal of the American Chemical Society》(中文名)上在线发表题为“SELEX-HTCFQ Platform:Developing DNA Enhancers of ADAR1 to Suppress ZBP1-Dependent Immunopathology”(SELEX-HTCFQ平台:开发ADAR1的DNA增强子以抑制ZBP1依赖性免疫病理)的研究论文。

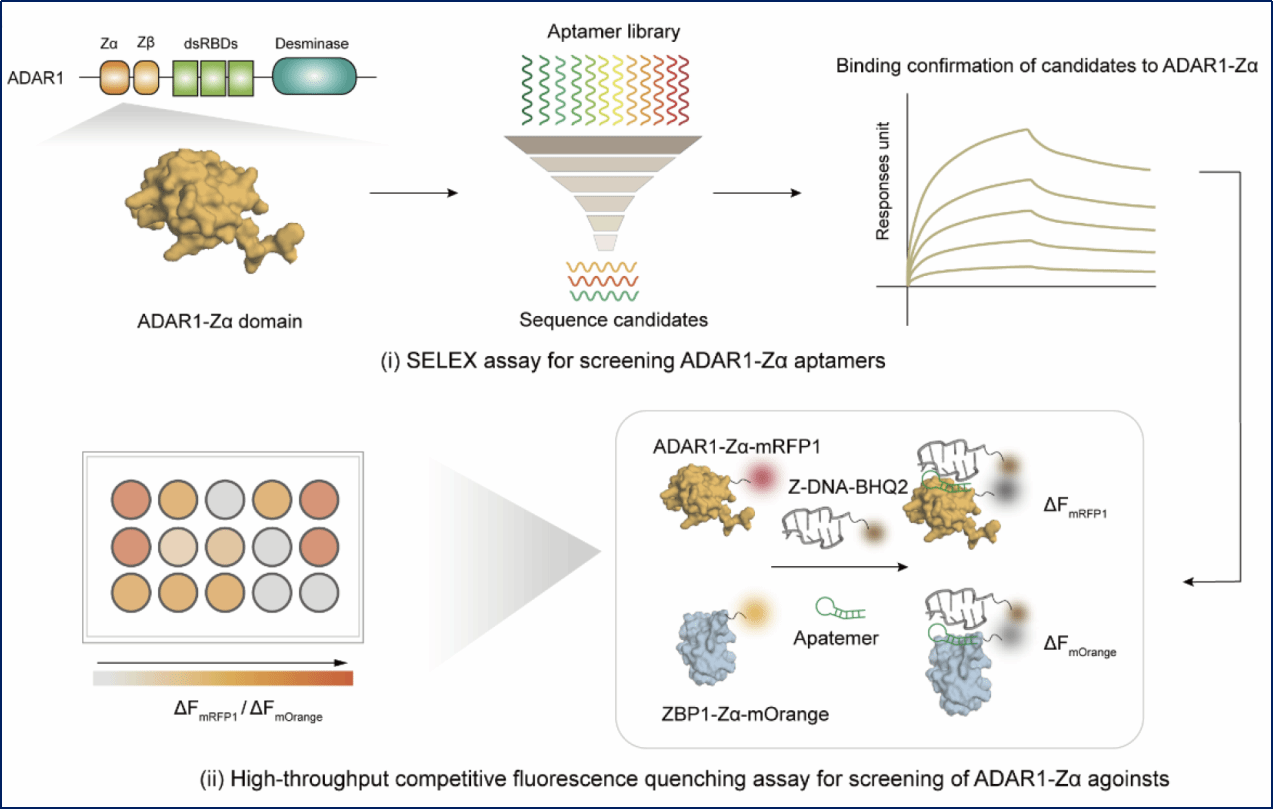
该研究报道了一种创新的SELEX-HTCFQ筛选平台,此平台能够将系统进化配体指数富集技术与高通量竞争性荧光淬灭技术相结合,用于高效识别具有功能结构域特异性的DNA适配体。该平台的突出创新在于其“双重筛选”策略:不仅评估适配体与靶蛋白ADAR1-Zα结构域的亲和力,还通过竞争性荧光淬灭实验定量评估其对ADAR1与ZBP1结合Z-DNA的选择性增强能力。这一设计超越了传统SELEX方法主要筛选高亲和力结合分子的局限,首次实现了在筛选阶段同步优化“功能增强”与“靶点选择性”,从而直接获得具有预定生物学功能的分子工具。
利用该平台,研究团队成功鉴定出适配体A4,它能够特异性增强ADAR1-Zα与Z-DNA的结合,同时竞争性抑制ZBP1-Zα与Z-DNA的相互作用。A4通过形成广泛的氢键网络与ADAR1-Zα结合,将其对Z-DNA的亲和力提高近10倍,从而在分子水平上实现了对ZBP1通路的选择性抑制,而非完全阻断,保留了ZBP1在免疫监视中的基础功能。
为进一步提升其治疗潜力,研究还创新性地开发了甘露糖化修饰的Man-A4,实现了对肺部免疫细胞的精准靶向和长效滞留。在流感病毒肺炎模型中,Man-A4展现出强大的抗炎和抗坏死性凋亡活性,实现了对病理炎症的精准干预,同时避免了系统性免疫抑制的副作用。
该研究不仅在方法学上为功能型适配体的筛选提供了全新范式,更在治疗策略上提出了“增强内源性抑制蛋白以精准调控免疫通路”的新理念,为炎症性疾病及细胞死亡相关疾病的治疗开辟了新的药物开发途径。
该成果以海南医科大学为第一完成单位。海南医科大学教师胡宇斯、南开大学博士研究生黄仁堂为共同第一作者,南开大学刘书琳教授为通讯作者。
原文链接:http://pubs.acs.org/doi/abs/10.1021/jacs.5c18671
