1.谢茂委图团队开发血小板搭载四面体框架核酸(TFNAs@PLT)实现肾损伤精准抗氧化治疗
1月1日,海南医科大学附属海南医院联合南京医科大学、常州市妇幼保健院等团队,在国际权威期刊《Theranostics》在线发表题为“Spatially selective clearance of inflammation‑mediated reactive oxygen species in injured kidney cells”的研究论文。

急性肾损伤与慢性肾病均以ROS过量累积为核心病理特征,传统抗氧化剂缺乏空间选择性,在清除有害ROS的同时也会干扰正常细胞所需的生理性ROS,如自噬信号分子。为解决这一难题,本研究将具有高效抗氧化能力的四面体框架核酸(TFNAs)装载到血小板(PLT)中,利用血小板对炎症信号(如TNF-α)的天然响应能力,实现了纳米药物在受损肾脏区域的定点富集和按需释放并淬灭ROS,同时保护正常细胞免受干扰。实验表明,TFNAs@PLT在体外可被TNF-α激活,释放TFNAs并有效清除脂多糖诱导的ROS爆发。在小鼠缺血再灌注(I/R)诱导的AKI模型中,TFNAs@PLT显著降低了血尿素氮和血清肌酐水平,减轻了肾小管上皮细胞的坏死、脱落及足细胞损伤。在阿霉素诱导的CKD模型中,TFNAs@PLT有效抑制了肾间质纤维化,减少了胶原沉积。机制研究进一步揭示,TFNAs@PLT在AKI中通过抑制NLRP3介导的Caspase-1/IL-1β通路以及Caspase-3/GSDME通路,减轻了炎症介导的细胞焦亡和凋亡;在CKD中则通过调控NLRP3/Caspase-1和TNF-α/NF-κB通路,缓解了肾脏纤维化进程。经TFNAs生物安全性评估显示,TFNAs@PLT对心、肝、脾、肺、肾等主要脏器无明显病理损伤,具备良好的生物相容性与临床转化潜力。
该研究首创血小板包裹四面体框架核酸纳米递送系统(TFNAs@PLT),利用血小板天然的炎症趋化特性,实现了对肾损伤部位活性氧(ROS)的精准清除,为急性肾损伤(AKI)与慢性肾病(CKD)提供安全高效的靶向治疗新策略。
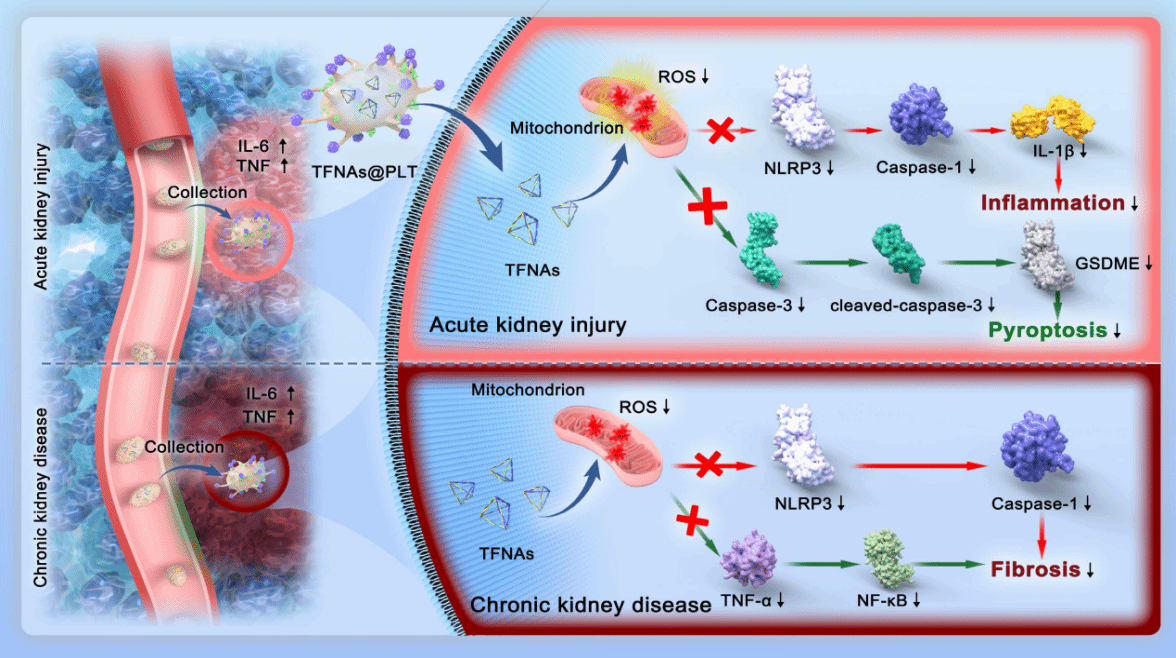
TFNAs@PLT治疗AKI与CKD的作用机制示意图
该研究以海南医科大学附属海南医院为第一完成单位,谢茂委副主任医师、符昕博士、兰宇飞博士为共同第一作者,冒志磊教授、何健教授、丁雪晶研究员为共同通讯作者。研究得到国家自然科学基金、海南省临床医学中心等项目资助。
原文链接:https://www.thno.org/v16p1466.htm
2.陈建强团队开发仿生“纳米活性氧风暴”平台,实现磁热诱导自噬增强铁死亡治疗胶质母细胞瘤
1月18日,海南医科大学第一附属医院放射科陈建强团队与海南大学生物医学工程学院吴锡龙团队合作,在国际知名学术期刊《Chemical Engineering Journal》在线发布了题为“Transforming glioblastoma treatment: Magnetothermal induction of biomimetic ROS storm agents for autophagy-enhanced ferroptosis”的研究论文。该研究开发了一种名为MDM的仿生纳米药物,通过磁热效应诱导自噬爆发,打破肿瘤氧化还原平衡,显著提升了胶质母细胞瘤(GBM)的铁死亡治疗效果。

胶质母细胞瘤(GBM)是中枢神经系统中最具侵袭性的恶性肿瘤,由于血脑屏障(BBB)的存在和其高度异质性,传统疗法效果受限,患者预后极差。铁死亡(Ferroptosis)作为一种铁依赖性的脂质过氧化驱动的程序性细胞死亡方式,为克服肿瘤耐药提供了新视角。然而,肿瘤细胞强大的抗氧化防御系统往往会抵消单一路径诱导的铁死亡效果。本研究开发的MDM 纳米平台由超顺磁性MnFe2O4核心、抗肿瘤药物双氢青蒿素(DHA)以及包覆的癌细胞膜(CM)组成。该系统具有以下核心优势:借助癌细胞膜的同源识别能力和磁场引导,MDM能高效跨越血脑屏障并主动靶向肿瘤病灶。在交变磁场(AMF)驱动下,MDM利用磁热效应加速类过氧化物酶、类谷胱甘肽氧化酶和类过氧化氢酶等催化活性,触发高通量活性氧(ROS)暴发。MDM释放的Mn、Fe离子与DHA协同作用,通过诱导铁蛋白自噬释放更多亚铁离子,并阻断 SLC7A11-GPX4抗氧化轴,从内、外两条路径同步瓦解肿瘤防御。凭借其超顺磁性,MDM 可作为T1-T2双模态核磁共振成像(MRI)造影剂,实现肿瘤的精准可视化及疗效实时监测。实验结果显示,在原位胶质母细胞瘤小鼠模型中,MDM 结合磁热治疗可使肿瘤抑制率达到95.37%,并将中位存活时间延长87.76%。同时,安全性评估证实该治疗方案未对主要器官及正常脑组织造成明显毒副作用。该工作为诱导胶质母细胞瘤细胞铁死亡建立了从机制创新到临床转化的新思路。
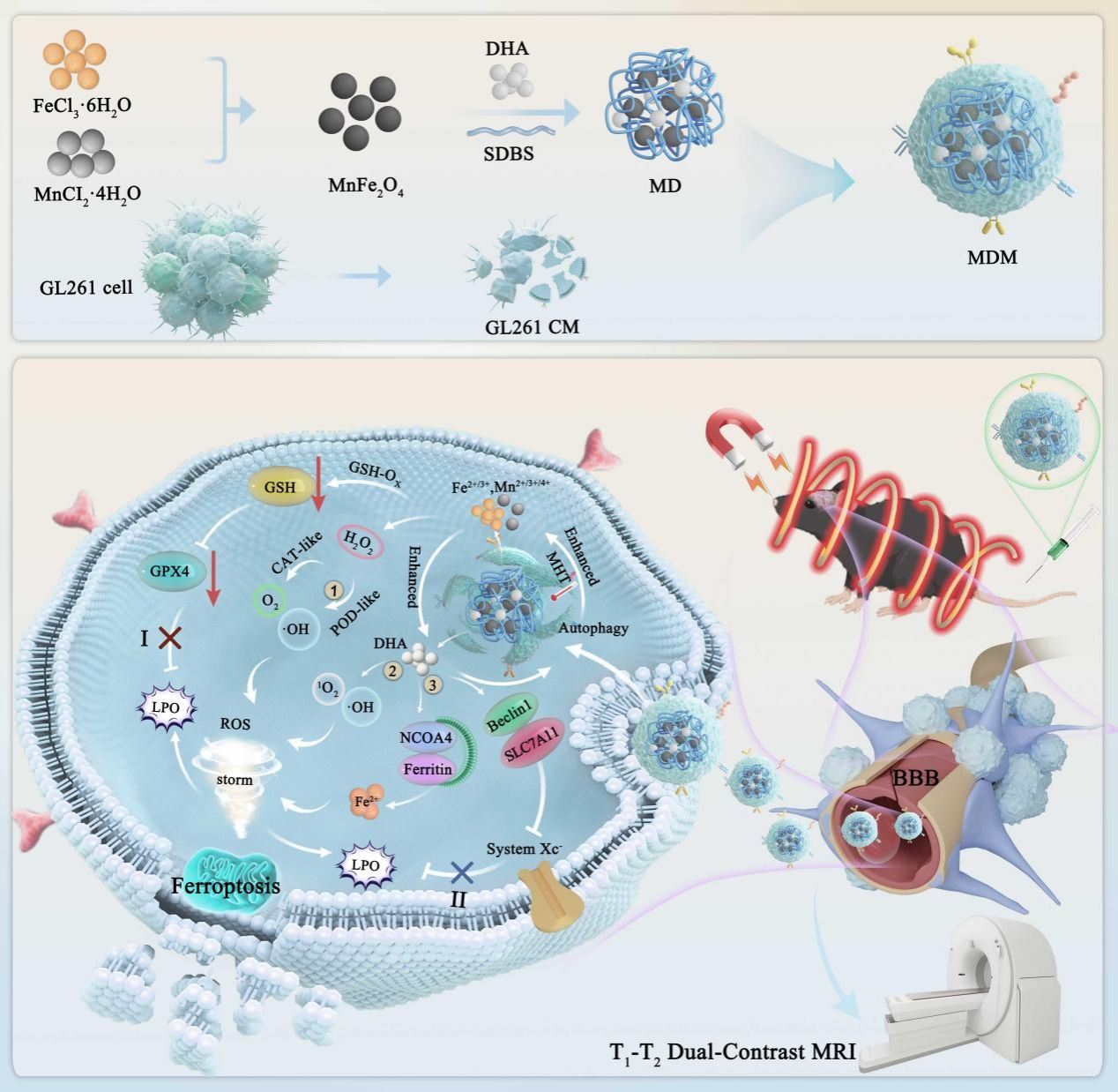
该论文以海南医科大学第一附属医院为第一单位,海南医科大学(海南省医学科学院)博士研究生杨小红、海南大学生物医学工程学院吴云娣博士、四川大学华西医院张健博士为该论文共同第一作者,海南医科大学第一附属医院放射科陈建强主任与海南大学生物医学工程学院吴锡龙教授为共同通讯作者。该研究得到了国家自然科学基金、海南省科技专项资金等项目的支持。
原文链接:https://doi.org/10.1016/j.cej.2026.173045
3.夏乾峰/田新龙团队系统提出破解微生物燃料电池“阳极困境”的优化策略与应用路径
1月20日,海南医科大学(海南省医学科学院)国家卫健委热带病防治重点实验室夏乾峰教授团队与海南大学田新龙教授团队合作在国际权威学术期刊《Renewable and Sustainable Energy Reviews》发表了题为“How to address the anode dilemma and explore future prospects of microbial fuel cells”的研究成果。该论文系统梳理了微生物燃料电池阳极界面的研究进展与发展方向,重新定义了微生物燃料电池的关键问题,为高效、稳定生物电化学界面的构建及相关领域的医工交叉研究提供了理论参考。

微生物燃料电池是一类利用微生物将有机物直接转化为电能的生物电化学系统。论文指出,阳极不仅是电子传递的关键界面,也是微生物黏附、生物膜形成和稳定运行的核心载体,其性能直接影响体系的整体输出。当前,该领域仍面临界面电子传递缓慢、生物膜稳定性不足、传质受限及规模化成本较高等挑战。研究突出“微生物—材料界面”的作用机制,围绕胞外电子传递、生物膜构建、材料生物相容性及界面调控等关键问题,系统总结了阳极微生物改造、材料优化、原位表征、多尺度模拟及综合评价体系等研究策略,为构建高效、稳定、可规模化的生物电化学界面提供了理论参考。值得关注的是,相关研究思路与生物医学领域中感染微环境调控、生物膜行为解析、医用材料界面设计及生物传感体系构建等方向具有重要交叉意义,可为感染性疾病诊疗相关功能材料开发和医工融合研究提供有益借鉴。
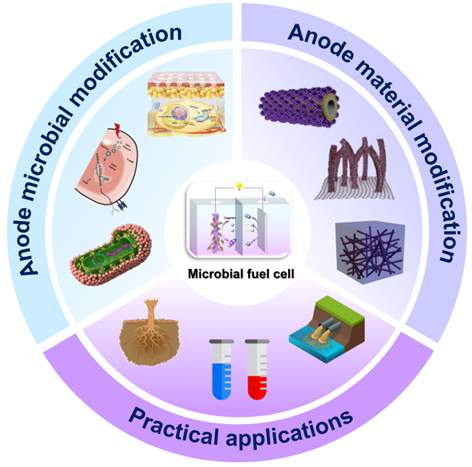
该成果以海南医科大学(海南省医学科学院)为第一完成单位,生命科学与医学技术学院刘玮博士为该论文的唯一第一作者,夏乾峰教授,旷代副研究员和海南大学田新龙教授为通讯作者。该研究受到国家自然科学基金、海南省重大科技专项等项目资助。
原文链接:https://doi.org/10.1016/j.rser.2026.116745.
4.马高恩团队发现糖尿病视网膜病变新机制:MDM2 SNP309G驱动异常血管生成
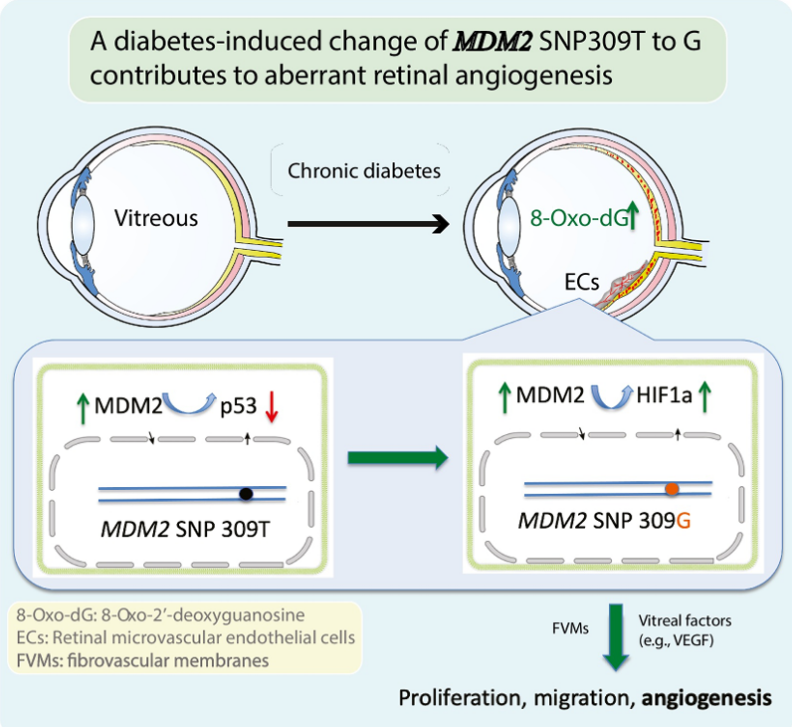
3月2日,海南医科大学第一附属医院马高恩团队在《Diabetologia》杂志接受发表题为“A diabetes‑induced change of MDM2 SNP309 T→G contributes to aberrant retinal angiogenesis”的研究论文。该研究发现MDM2 SNP309 T→G变异与增殖性糖尿病视网膜病变(PDR)中的异常血管生成密切相关。

研究通过分子生物学技术,在PDR患者纤维血管膜中检测到该变异,并发现玻璃体液中氧化DNA损伤标志物8-oxo-2'-脱氧鸟苷水平显著升高。高糖环境下,该变异会抑制8-氧鸟嘌呤DNA糖苷酶表达,促进MDM2蛋白水平升高,进而增强新生血管的形成。在小鼠模型中,携带MDM2 SNP309G的小鼠表现出更严重的视网膜新生血管形成。这一发现提示糖尿病诱导的MDM2 SNP309 T→G促进病理性新生血管生成的机制,为靶向MDM2治疗糖尿病视网膜病变提供新思路。
该成果以海南医科大学(海南省医学科学院)为第一完成单位,海南医科大学第一附属医院眼科马高恩主任为该论文的共同第一作者(排名第一),哈佛医学院雷和田教授,中南大学湘雅二医院罗静教授和深圳市眼科医院闫晓河教授为通讯作者。该研究受到国家自然科学基金、高端外国专家引进计划、海南省自然科学基金、广东省基础与应用基础研究基金等项目资助。
原文链接:https://pubmed.ncbi.nlm.nih.gov/41770245/
5.陈旺生团队提出多模态融合新方法实现高级别胶质瘤精准分割与预后预测
3月,海南医科大学附属海南医院放射科陈旺生团队在《Information Fusion》在线发表题为“Advanced 3D segmentation and prognostic prediction of high-grade glioma via multimodal MRI, pathological imaging, and Point Cloud data integration”的研究论文。该研究针对高级别胶质瘤高度异质性及传统方法依赖单模态影像、分割与预后分析割裂等问题,提出一种融合多模态影像与病理信息的深度学习框架,实现肿瘤分割与生存预测的协同优化。

高级别胶质瘤是一类侵袭性强、复发率高、预后极差的恶性脑肿瘤。传统影像分析方法多依赖单一MRI图像,难以全面反映肿瘤的复杂结构与生物学行为,限制了诊断精度与预后评估能力。本研究通过整合多序列MRI(T1、T2、FLAIR)与病理图像数据,构建多模态数据自适应融合模块,并结合改进的三维U-Net网络,实现对肿瘤空间结构的高精度分割。同时,研究进一步融合肿瘤形态特征、纹理特征及临床信息,建立深度神经网络模型,实现患者生存期的精准预测。研究结果表明,该方法在自建数据集上取得优异表现,准确率达91.34%,F1值达94.53%,显著优于传统方法。此外,消融实验进一步证实,多模态融合与分割—预测联合建模策略对性能提升具有关键作用。该研究首次实现了胶质瘤影像分析中“分割与预后预测一体化“的深度学习框架,为复杂肿瘤的智能分析提供了新范式。该成果为胶质瘤精准诊疗提供了重要技术支撑,有望在手术规划、疗效评估及个体化治疗决策中发挥重要作用。
该成果以海南医科大学附属海南医院为第一完成单位,由海南医科大学(海南省医学科学院)等多单位合作完成,体现了放射科、神经外科与病理学等多学科交叉优势。研究工作得到国家自然科学基金等项目资助。
论文链接:https://doi.org/10.1016/j.inffus.2025.103658
6.李其富/黄灿华团队构建脑靶向水飞蓟素纳米平台协同抑制线粒体增效GBM免疫治疗
4月,海南医科大学(海南省医学科学院)李其富团队与四川大学华西医院生物治疗国家重点实验室黄灿华团队合作在《Materials Today Bio》在线发表了题为“ Brain-Targeting Nanoplatform Repurposing Silymarin for Enhanced GBM Immunotherapy via Synergistic Mitochondrial Suppression ”的研究论文。该研究首次将肝保护药物水飞蓟素通过脑靶向纳米递送系统重新用于神经胶质母细胞瘤(GBM)的治疗,通过协同诱导线粒体功能障碍,激活AMPK和cGAS-STING通路,显著增强抗肿瘤免疫应答,为GBM免疫治疗提供了全新的药物重定位策略。

GBM是中枢神经系统最常见且恶性程度最高的原发性肿瘤,由于血脑屏障(BBB)的存在和高度免疫抑制的肿瘤微环境,现有免疫检查点抑制剂疗效十分有限。本研究团队基于“老药新用”策略,将具有抗炎、保肝作用的水飞蓟素与光敏剂二氢卟吩e6(Ce6)进行纳米共组装,并修饰以脑靶向配体乳铁蛋白(LF),成功构建了多功能纳米平台L-S-TCe6/NPs。
该平台中,乳铁蛋白通过结合低密度脂蛋白受体相关蛋白1(LRP1)介导跨血脑屏障转运;三苯基膦(TPP)修饰的Ce6(TCe6)可靶向线粒体并在660 nm近红外光照射下产生大量活性氧(ROS);水飞蓟素则抑制肿瘤细胞糖酵解,进一步加剧线粒体损伤。两者协同作用导致线粒体膜电位丧失、ATP耗竭,并激活AMPK信号通路,下调免疫检查点PD-L1的表达;同时,ROS引起的DNA损伤激活cGAS-STING通路,促进树突状细胞成熟和T细胞浸润。体内原位GBM模型显示,L-S-TCe6/NPs联合光照可显著抑制肿瘤生长,延长小鼠生存期,并降低调节性T细胞(Treg)水平。双侧皮下瘤模型进一步证实该平台可诱导远端抗肿瘤免疫效应,原发灶抑瘤率达97.11%,远端灶达78.40%。
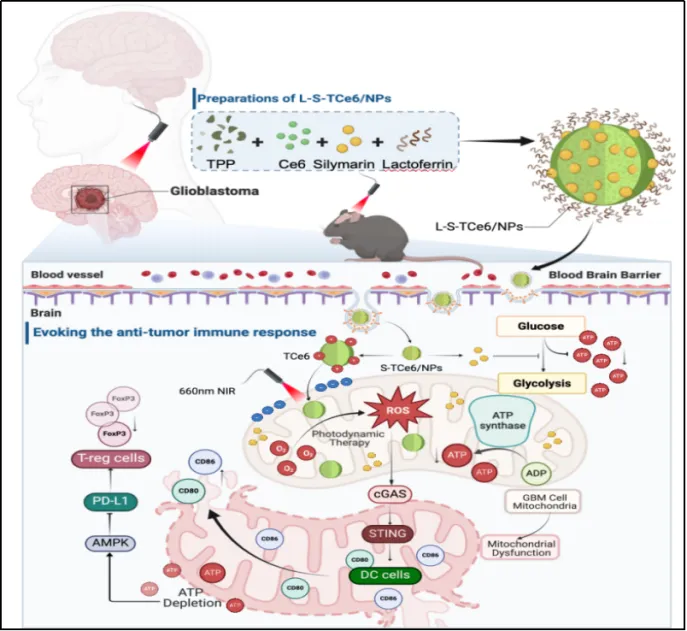
该论文以海南医科大学(海南省医学科学院)为第一单位,海南医科大学刘家琪博士与四川大学华西医院程文婷博士为共同第一作者,海南医科大学李其富教授与四川大学华西医院生物治疗国家重点实验室黄灿华教授为共同通讯作者。该工作受到国家自然科学基金、四川省科技计划、海南省临床医学中心等项目的资助。
原文链接:https://doi.org/10.1016/j.mtbio.2026.102951
7.高炳淼团队发现新型抗癌环肽为非小细胞肺癌治疗提供新思路
海南医科大学药学院高炳淼教授课题组与广西大学吴勇课题组合作在国际权威期刊《Phytomedicine》发表研究论文“Characterization of cyclotide Vdif A from Viola diffusa inhibits non-small cell lung cancer cells via regulation of CKS2”从传统药用植物Viola diffusa中成功分离出一种新型环肽 Vdif A,该化合物对非小细胞肺癌(NSCLC)表现出显著抑制作用,并首次揭示了其通过调控细胞周期蛋白 CKS2 发挥抗癌作用的新机制。

非小细胞肺癌约占肺癌病例的85%,现有疗法常面临耐药困境。团队从中国南方传统药用植物七星莲(Viola diffusa)中共鉴定出30种天然环肽,并从中筛选出活性最强的Vdif A。细胞实验显示,Vdif A对非小细胞肺癌A549细胞的半数抑制浓度(IC₅₀)仅为0.455微摩尔,能够诱导癌细胞周期停滞于S期、激活线粒体凋亡通路并造成DNA损伤。蛋白质组学分析进一步发现,Vdif A可显著下调细胞周期关键调控蛋白CKS2的表达,基因敲低实验证实抑制CKS2可增强其抗癌效果。荷瘤小鼠实验中,Vdif A以2-4 mg/kg剂量给药后肿瘤生长抑制率达46.58%,且未见明显系统性毒性。研究团队指出,这是首次证明植物环肽可通过调控胞内蛋白表达发挥抗肿瘤作用,为环肽类药物的机制研究及非小细胞肺癌新药开发提供了重要参考。
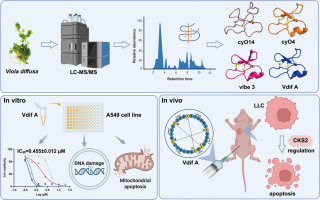
该论文以海南医科大学(海南省医学科学院)为第一单位,海南医科大学(海南省医学科学院)高炳淼教授与广西大学罗素兰教授和吴勇教授为共同通讯作者,广西大学硕士生何发伟和博士生何全阔为第一作者。该工作受到国家自然科学基金和热带药物创新与转化教育部工程研究中心开放课题等项目资助。
原文链接:https://doi.org/10.1016/j.phymed.2026.158146
8.谭静团队研究发现抑癌基因BAP1作用机制,为BAP1失活突变的恶性肿瘤治疗提供新方案
4月1日,海南医科大学(海南省医学科学院)谭静教授团队联合新加坡国立癌症中心、杜克-新加坡国立大学医学院的郑敏展教授团队,在《Science Translational Medicine》杂志发表题为“Uncovering BAP1 Deubiquitination Landscape Enhances Mechanism Elucidation and Therapeutic Precision for BAP1-Deficient Pan-Cancers”的重磅研究,揭示了BAP1在分子水平上的功能,并提出了一种新的治疗策略,可延缓携带BAP1突变的间皮瘤、葡萄膜黑色素瘤、胆管癌和肾透明细胞癌的进展。

BAP1(BRCA1相关蛋白1)是一种抑癌基因,通过去泛素化作用移除靶蛋白上错误的泛素标签,保护关键蛋白免遭降解,维持DNA修复和细胞周期稳态。其缺失会导致修复蛋白降解、有害蛋白蓄积,引发DNA修复缺陷和细胞周期失控,从而驱动癌症发生。BAP1功能缺陷可驱动间皮瘤、葡萄膜黑色素瘤、胆管癌及肾透明细胞癌(全球每年超40万新发)的恶性进展。传统化疗、免疫及放疗效果有限,尽管抑癌基因BAP1失活突变与多种恶性肿瘤发生发展密切相关,但其具体机制尚不明确。
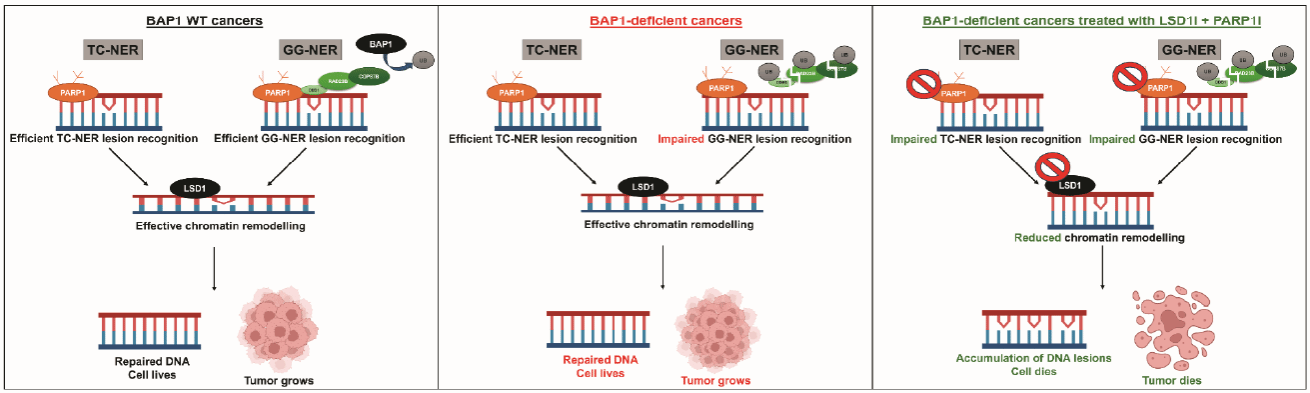
BAP1失活型肿瘤靶向治疗策略示意图
在该研究中,为深入解析BAP1的功能,研究人员首先建立了四种BAP1缺陷型肿瘤(间皮瘤、葡萄膜黑色素瘤、胆管癌、肾透明细胞癌)的细胞系、类器官及动物模型。利用质谱分析、ChIP-seq与ATAC-seq等技术,发现BAP1在全局基因组核苷酸切除修复(修复大片段DNA损伤的关键通路)中发挥重要作用。机制上,BAP1通过去除DDB1、RAD23B和COPS7B三个DNA损伤识别蛋白上的泛素标签,保护其免遭降解,从而维持DNA修复及正常细胞功能。
随后,研究团队对422种抗癌药物进行高通量筛选,旨在识别可特异性靶向BAP1失活型癌细胞的化合物。结果显示,LSD1抑制剂SP2509能高效杀伤BAP1缺陷型癌细胞的同时,能有效避免伤害正常细胞;PARP1抑制剂奥拉帕利在小鼠模型中可减缓肿瘤生长并延长生存期。两者联用表现出显著协同效应,进一步抑制癌细胞扩散。上述发现均在细胞实验、患者来源类器官及小鼠模型中得到了验证。
综上所述,该研究揭示了BAP1蛋白修复DNA和调控细胞功能的新方式,并为BAP1缺陷型恶性肿瘤提出了富有前景的治疗新策略,有望填补目前针对BAP1缺陷型肿瘤尚无获批疗法的治疗空白。
海南医科大学(海南省医学科学院)/中山大学肿瘤防治中心谭静教授,新加坡国立癌症中心、杜克-新加坡国立大学医学院郑敏展教授/Hong Jing Han博士为本文通讯作者。
原文链接:DOI: 10.1126/scitranslmed.adr6668
9.金红林教授科研团队发表重磅成果:用“胆固醇调控”激活纳米疫苗抗癌新策略
4月16日,海南医科大学生命科学与医学技术学院金红林教授团队联合中国科学院长春应用化学研究所和美国纽约州立大学布法罗分校合作在国际学术期刊《Nature Nanotechnology》在线发表了题为“Enhancing Antitumor Nanovaccine Efficacy via Integrated Cholesterol Modulation In Situ”的研究成果。

该研究聚焦肿瘤疫苗“免疫激活不强”这一核心难题,创新性地从树突状细胞膜胆固醇这一关键因素入手,提出通过降低细胞膜胆固醇水平来增强抗原递呈能力的新策略。基于这一发现,研究团队设计并构建了一种兼具“抗原递送+胆固醇调控”双重功能的纳米疫苗体系,能够实现对树突状细胞膜胆固醇的原位调控。该体系在递送抗原的同时,可有效降低细胞膜胆固醇水平,协同增强抗原的加工与递呈能力。研究首次证实,膜胆固醇耗竭能够显著提升免疫激活效率。
进一步研究发现,这一过程如同为免疫细胞间的相互作用“打开加速通道”:不仅增强了树突状细胞与T细胞的接触及免疫突触的形成,还通过重塑膜胆固醇微结构并阻断胞葬通路,显著提升CD8⁺ T细胞的增殖能力与抗肿瘤功能。该策略在多种肿瘤模型中均实现了显著的抑瘤效果,为新一代高效肿瘤纳米疫苗的研发提供了重要方向。
综上所述,靶向调控树突状细胞膜胆固醇水平,不仅能系统性提升抗原递呈效率,还可重塑免疫细胞间的相互作用模式,从而实现对抗肿瘤免疫反应的精准放大。该研究为开发新一代高效肿瘤纳米疫苗及免疫治疗策略提供了重要的理论依据与实验基础
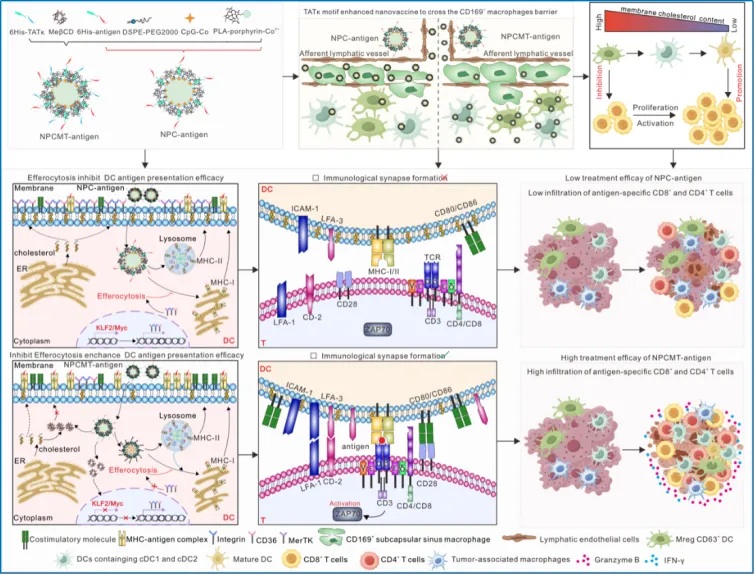
胆固醇调控与细胞穿透协同增强纳米疫苗抗肿瘤免疫的示意图
本研究由金红林教授团队牵头完成,课题组邓紫晗博士生、卢利森副研究员和徐天兵博士生为本文的共同第一作者。华中农业大学生物医学与健康学院孙耀教授、中国科学院长春应用化学研究所丁建勋教授与美国纽约州立大学布法罗分校Jonathan F. Lovell教授为本文的共同通讯作者。
原文链接:https://www.nature.com/articles/s41565-026-02153-w
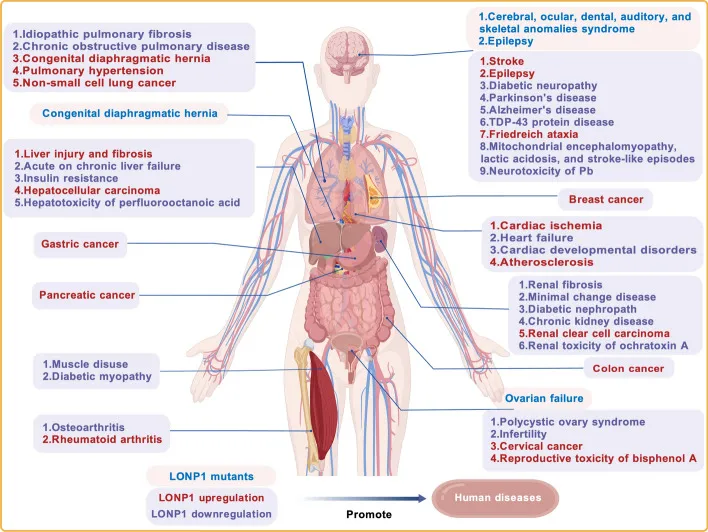
10.李明康团队最新综述LONP1在人类疾病中的作用:分子机制与治疗潜力
1月31日,海南医科大学附属海南医院心血管内科李明康博士在国际权威期刊《Cellular & Molecular Biology Letters》发表题为“LONP1 in human diseases: molecular mechanisms and therapeutic potential”的综述论文。该综述系统总结了线粒体蛋白酶(LONP1)通过维持线粒体蛋白稳态与基因组完整性,在肿瘤、心脑血管及神经退行性疾病中的多维调控机制,并评估了靶向治疗的潜力,为线粒体稳态失衡相关疾病的机制研究与精准治疗提供了理论依据。

线粒体通过整合分子伴侣、泛素途径、UPRmt、蛋白酶、囊泡与自噬等多种机制,形成复杂的线粒体蛋白质量控制(PQC)系统;其中,分布于不同区室的线粒体蛋白酶作为核心执行者,通过特异性底物识别与降解,在蛋白质成熟、复合物组装及异常蛋白清除中发挥不可替代的作用。 哺乳动物线粒体包含45个具有严格区室特异分布的蛋白酶,其中定位于基质的Lon蛋白酶1(LONP1)因其独特的结构特征和多功能特性而成为研究重点。作为AAA+蛋白酶超家族成员,LONP1从大肠杆菌到人类的高度保守,其六聚体环结构具有复杂的机械工作机制:N端识别并结合底物,AAA+结构域驱动底物展开,通过ATP水解将展开的多肽链送达C端丝氨酸蛋白酶活性中心进行降解,这种“结合-展开-运输-切割”四合一的机制使其能够高效去除氧化损伤的蛋白质、错误组装的酶复合物和异常蛋白,是维持线粒体基质蛋白稳态的第一道防线。该综述系统地将LONP1的生物学景观从发现、结构和功能方面划分开来,阐明LONP1在不同人类疾病微环境中的功能切换机制,同时整合了其在多种人类疾病情境中病理生理双重性的新兴证据,探索了其作为相关疾病治疗靶点的潜力。
该论文以海南医科大学附属海南医院为第一单位,海南医科大学附属海南医院心血管内科李明康博士为该论文第一作者兼共同通讯作者,东南大学附属中大医院张文康博士和海南省妇女儿童医学中心吴亚妹主治医师为共同通讯作者。该工作受到国家自然科学基金委、海南省临床医学中心资助。
原文链接:https://pubmed.ncbi.nlm.nih.gov/41620670/
11.高炳淼团队发表芋螺毒素最新综述:从海洋“猎手”到新药研发
2月5日,海南医科大学药学院高炳淼教授课题组与深圳大学及华大海洋(研究院)石琼教授课题组合作在国际权威期刊《Zoological Research》在线发表综述论文“From marine predator to pharmacology: Conotoxin diversity, discovery, and therapeutic potential”,系统梳理了芋螺毒素(Conotoxins)的多样性来源、发现技术路线、关键药理靶点及其治疗转化潜力,为海洋天然产物与肽类药物研发提供了重要的综合性参考。

该综述以“捕食生态—毒素模块进化—离子通道/受体靶向—多组学发现—药物优化”为主线,系统回答了芋螺毒素为何具备高效、强效及高亚型选择性,以及如何加速“从毒液到药物”的转化。
核心内容包含四个方面:第一,从生态角度揭示毒素多样性与捕食策略的耦合关系。芋螺按食性分为食鱼、食蠕虫和食软体动物三类,不同捕食策略对应特定药理模块的扩张,如食鱼类芋螺富集快速起效的离子通道靶向毒肽,并借助系统发育与齿舌形态分析,直观呈现“形态—功能—毒素”关联。第二,系统梳理神经药理学关键靶点,涵盖电压门控钠、钾、钙通道(尤其是Ziconotide靶点Caᵥ2.2)及烟碱型乙酰胆碱受体,以表格汇总代表性毒素的作用机制、潜在应用与物种来源。第三,聚焦方法学革新,将当前发现路径归纳为传统纯化筛选、基因重组表达和毒素组学三大策略;指出序列获取速度提升后,瓶颈转向功能去孤儿化及可开发性评估。第四,面向转化应用,强调结构–活性关系(SAR)与计算设计对药物优化的推动作用,包括环化、非天然氨基酸引入、构象限制等策略,并兼顾稳定性、半衰期、免疫原性及规模化生产,展望计算与工程平台在下一代毒肽药物研发中的关键角色。

芋螺的全球分布与形态多样性
该论文以海南医科大学(海南省医学科学院)为第一单位,海南医科大学药学院毛楷林博士为第一作者,海南医科大学药学院高炳淼教授和深圳大学及华大海洋(研究院)石琼教授为共同通讯作者。该工作受到海南省国际科技合作研发项目和热带药物创新与转化教育部工程中心开放课题资助。
原文链接:https://doi.org/10.24272/j.issn.2095-8137.2025.553
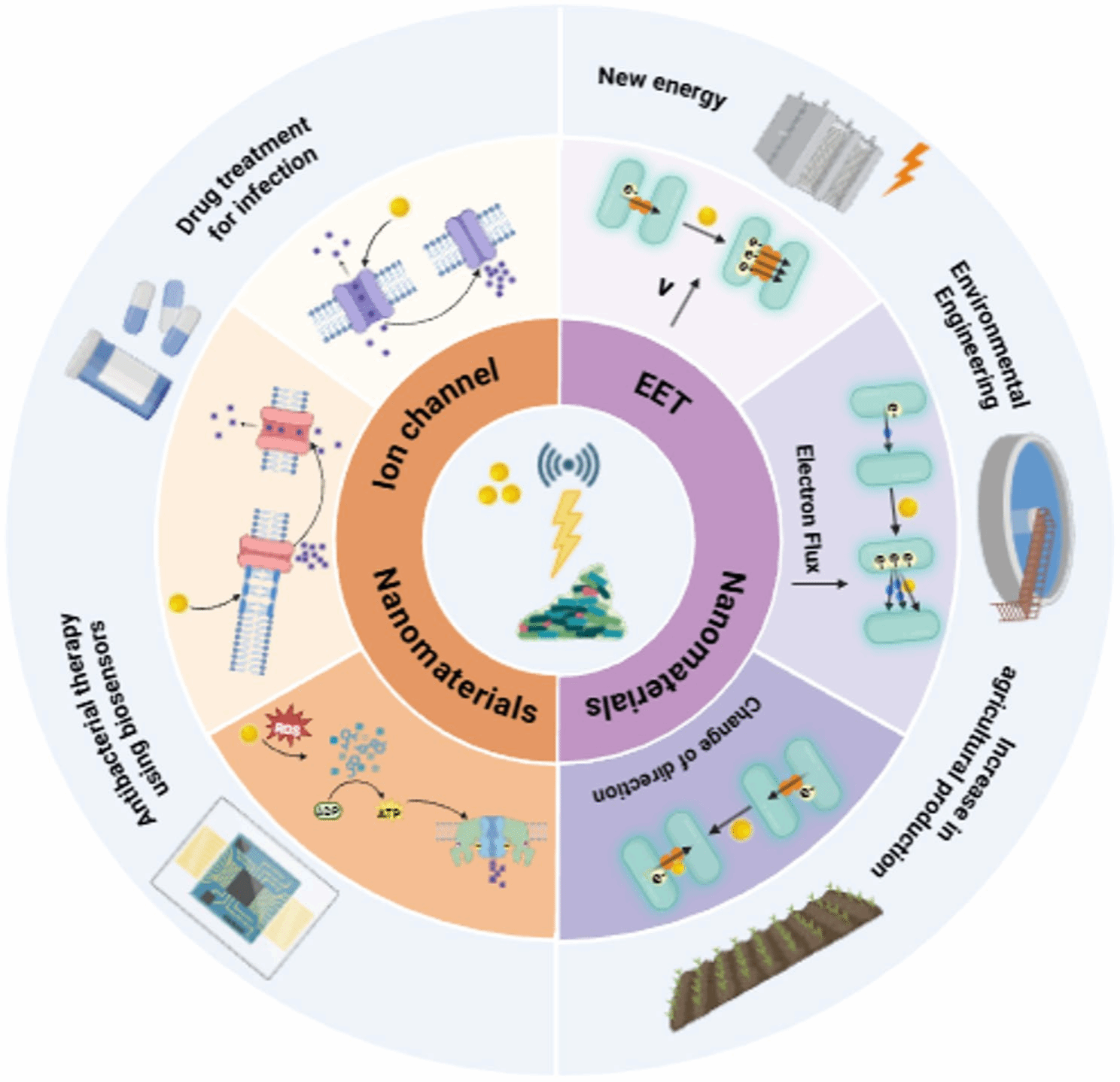
12.王琳琳团队综述:纳米材料调控细菌生物膜电化学信号传导的机制与应用前景
2月16日,海南医科大学附属海南医院口腔科王琳琳团队在国际期刊《Journal of Nanobiotechnology》在线发表了题为“Nanomaterials as electrochemical regulators of bacterial biofilms through the modulation of extracellular electron transport and ion channels”的综述论文。该综述系统梳理了纳米材料通过细胞外电子传递与离子通道两条核心通路调控细菌生物膜电化学通讯的分子机制,并总结了其在抗生物膜治疗、环境修复及合成生物学等领域的应用潜力,为纳米技术干预微生物群体行为提供了系统性理论框架。

细菌生物膜依赖电化学信号网络调控群体行为。传统观点关注群体感应等化学信号,近年发现细胞外电子传递与离子通道在代谢同步、资源分配及防御中同样关键,如何精准调控仍是重要挑战。本综述首次整合双通路,解析纳米材料调控生物膜电化学通讯的两种模式:电子传递通路:纳米材料通过调节/模拟细胞色素c、改变氧化还原电位以重导电子流、优化核黄素等介体,提升电子通量。离子通道通路:纳米材料通过物理阻塞、膜力学干扰或诱导活性氧,调控钾/钙通道动力学,干扰长程电信号传播。应用层面,该综述指出:离子通道阻断剂(如部分钙通道阻滞剂)可协同抗生素抗生物膜;纳米材料修饰电极能显著提升微生物燃料电池在废水处理与石油污染修复中的功率密度;调控细胞外电子传递可增强植物根际促生菌代谢,减少化肥依赖;合成生物学已利用电信号构建“活体电路”,实现布尔逻辑运算。
尽管前景广阔,该综述指出研究局限:多限于实验室条件、分子机制不明、安全评估不足且缺全球监管。未来需解码电信号规则、发展可降解纳米材料、构建宿主-微生物电化学对话模型。
该论文以海南医科大学(海南省医学科学院)为第一单位,海南医科大学口腔医学院硕士研究生方可熠、海南医科大学附属海南医院井刚主治医师为共同第一作者,王琳琳副主任医师为通讯作者。该工作得到海南省自然科学基金、海南医科大学附属海南医院院级项目及海南省教育厅科研项目的资助。
原文链接:DOI:10.1186/s12951-026-04152-4
13.郭峻莉/揭伟/张书娅系统阐释心肌缺血再灌注后的先天免疫反应机制与转化挑战
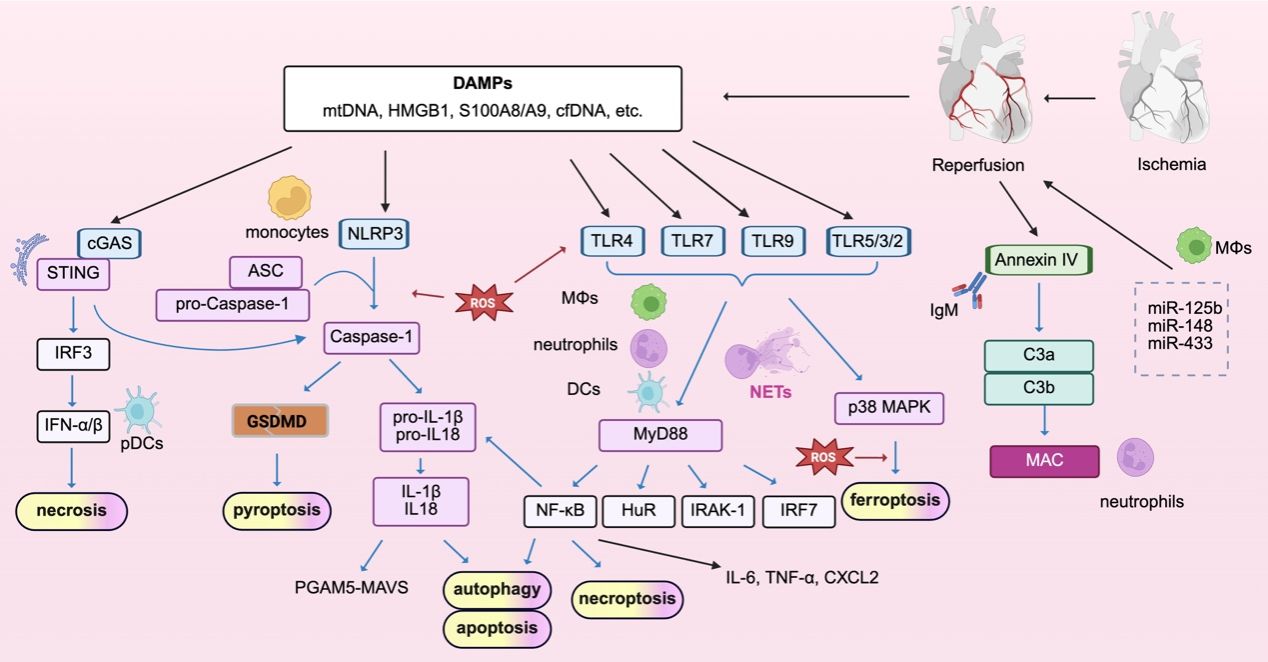
3月14日,海南医科大学海南省热带心血管病研究重点实验室/心血管病研究所郭峻莉/揭伟/张书娅等在国际知名期刊《Pharmacology & Therapeutics》在线发布了题为“Innate immune responses following myocardial ischemia and reperfusion: Evidence, mechanisms, and translational challenges”的论文,系统总结了心肌缺血再灌注损伤过程中先天免疫系统的关键作用机制,并对相关治疗策略的临床转化前景进行了深入分析。

急性心肌梗死是严重威胁人类健康的重要疾病,尽早开通闭塞冠状动脉、恢复心肌血流灌注是目前最有效的治疗方式,但大量患者在成功再灌注后仍会出现持续性心肌损伤、心功能下降及心力衰竭等不良结局,即心肌缺血再灌注损伤。近年来研究表明,先天免疫系统异常激活在这一过程中发挥关键作用。该论文围绕心肌缺血再灌注后的免疫炎症反应展开系统综述,指出受损心肌释放的损伤相关分子可迅速激活中性粒细胞、单核细胞、巨噬细胞及树突状细胞等先天免疫细胞,诱导炎症因子释放、氧化应激增强和微循环障碍,从而加重心肌损害。同时,文章强调免疫反应具有“双重效应”,在疾病后期部分免疫细胞又可促进坏死组织清除、血管新生及心肌修复。
研究进一步梳理了NLRP3炎症小体、cGAS-STING信号通路、补体系统、趋化因子轴及中性粒细胞胞外诱捕网等关键分子机制,并总结当前国际上围绕上述靶点开展的免疫调控治疗研究进展。作者指出,未来心肌梗死治疗策略应从传统单纯恢复血流灌注,逐步发展为结合病程阶段与患者个体特征的精准免疫干预模式,以实现更高水平的心肌保护和功能恢复。该研究成果发表于国际知名期刊,彰显了海南医科大学在心血管疾病基础研究、炎症免疫调控及转化医学领域持续提升的科研实力,也为我国心肌梗死精准治疗策略的探索提供了重要理论支撑。
该论文以海南医科大学为第一单位,海南医科大学青年教师张书娅博士、海南医科大学第一附属医院杜鹏举医生、海南医科大学硕士研究生张成为该论文共同第一作者,通讯作者是海南医科大学的郭峻莉教授、东南大学施国平教授、海南医科大学揭伟教授为共同通讯作者。该工作受到国家自然科学基金委、中国科学院等单位资助。
原文链接:https://doi.org/10.1016/j.pharmthera.2026.109026
14.于法标团队系统综述了近红外I/II区荧光CDs的合成、光学性能调控及其生物医学应用
3月15日,海南医科大学生命科学与医学技术学院于法标团队在《Coordination Chemistry Reviews》发布了题为“Near-infrared I/II fluorescent carbon dots: tailoring synthesis and optical properties for biomedical applications”的综述文章。该综述系统总结了近红外碳点(NIR‑CDs)的制备策略(包括前驱体筛选、反应优化及合成后修饰)、深入探讨了其发光机制(碳核态、表面态、分子态贡献)及光学性能调控方法(杂原子掺杂、表面工程、自组装等),并评述了其在生物传感、深层成像和协同光疗中的应用。针对NIR-CDs当前面临的挑战,并提出了面向临床转化的未来发展方向,旨在为功能性碳纳米材料的设计提供整体视角。

近红外碳点(NIR CDs)主要采用水热、溶剂热或微波辅助热解等“自下而上”策略,以含大π共轭或杂原子的前驱体(如柠檬酸、苯二胺、有机染料及生物质)为原料,通过调控溶剂、温度、时间及pH,实现发射波长向NIR I/II窗口拓展。当前核心在于前驱体分子工程与杂原子掺杂协同优化尺寸、共轭程度及表面化学,但批次重现性差、构效关系不明仍是瓶颈。发光机制源于碳核态、表面态、分子态及交联增强发射效应,sp⟡共轭域主导红移。通过杂原子(N、S、Se、金属)掺杂、表面修饰、自组装及异质复合等策略,可优化波长、量子产率与多功能集成。
NIR CDs具有低毒、高光稳定及深层组织穿透优势,已用于生物传感、近红外成像、光热/光动力治疗及诊疗一体化,实现灵敏检测、高分辨成像、协同抗肿瘤/抗菌及多功能纳米平台构建。挑战在于NIR II区量子产率低、安全性/代谢不清、规模化制备差。未来需结合机器学习、发展精准表面工程、建立标准化体系,并推进药代与毒理评估,助力临床转化。
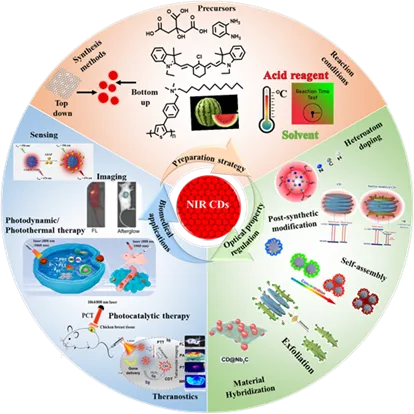
IR- CDs的合成策略、光学调控及生物医学应用示意图
该综述以海南医科大学(海南省医学科学院)为第一完成单位,第一作者为杜芳芳副研究员,通讯作者为于法标教授和戴宏杰院士。
原文链接:https://doi.org/10.1016/j.ccr.2025.217460
