免疫系统是人体抵御外来病原体的第一道防线,其中CD8+ T细胞是介导免疫应答的核心力量。静息状态下,初始CD8+ T细胞在抗原刺激下被激活,通过T细胞受体(TCR)发出信号,启动一系列反应,进而增殖并分化为效应细胞。在这一过程中,免疫系统需要保持精妙平衡:既要确保T细胞高效杀敌,又要防止其过度活化而伤及自身。然而,TCR信号如何启动负向调控以限制CD8+ T细胞效应反应,其分子机制仍不明确。
2026年3月24日,海南省医学科学院的程金科和上海交通大学医学院贺兼理团队在Cell Reports 在线发表了题为TCR-NF-κB signaling activates the SENP1-NR4A1 axis to fine-tune effector activation of CD8+ T cells的研究论文。该论文揭示了TCR-NF-κB信号通路可特异性诱导SENP1(SUMO特异性蛋白酶1)的表达。SENP1作为该通路的下游靶点,对TCR介导的CD8+ T细胞活化发挥负向调控作用。

研究人员首先观察到,小鼠初始CD8+ T细胞在体外经T细胞抗原受体(TCR)刺激后, SENP1表达显著增加,且这一上调可被TCR抑制剂以及NF-κB抑制剂显著阻滞,证实SENP1受TCR-NF-κB信号通路调控。研究人员随即构建了T细胞特异性敲除Senp1的cKO小鼠,发现效应记忆型CD8+ T细胞(CD44high CD62Llow)的数目在cKO小鼠中明显增多。进一步分离初始CD8+ T细胞并经抗CD3/CD28抗体刺激后,SENP1缺失的CD8+ T细胞中活化标志物(CD25、CD44、CD69)阳性比例显著升高,效应细胞因子(IFN-γ、TNF-α、IL-2)及颗粒酶B的产生亦明显增加。同时,SENP1缺失显著增强CD8+ T细胞的增殖能力。为探究SENP1调控CD8+ T细胞活化的分子机制,研究人员分离了cKO小鼠及对照小鼠的CD8+ T细胞进行转录组测序。结果显示,SENP1缺失后上调的基因显著富集于T细胞活化、细胞毒性及淋巴细胞增殖等相关通路。进一步分析激活动力学,SENP1缺失的活化CD69+ CD8+ T细胞在TCR刺激后IL-2产生能力显著强于对照细胞,且该差异在活化过程中持续存在。使用SUMO化抑制剂TAK981可显著逆转SENP1缺失所致的IL-2、CD25、CD44及CD69上调,证实SENP1通过去SUMO化修饰抑制CD8+ T细胞活化。
那么SENP1如何通过其去SUMO化修饰功能负向调控CD8+ T细胞活化?转录因子NR4A1作为CD8+ T细胞效应基因表达的关键负调控因子且存在SUMO化修饰,成为SENP1下游的潜在靶点。为验证这一假设,研究人员首先比较了SENP1缺失与NR4A1敲除CD8+ T细胞的转录谱特征。结果显示,SENP1缺失细胞中上调的基因与NR4A1调控的基因集高度重合,提示SENP1的抑制作用依赖于NR4A1活性。进一步实验证实,SENP1在CD8+ T细胞中亦介导NR4A1的去SUMO化修饰。为明确NR4A1受SUMO化修饰的关键位点,研究人员通过生物信息学预测、定点突变分析以及功能实验,证实NR4A1 K104位点的去SUMO化修饰是SENP1负向调控CD8+ T细胞活化的关键分子事件。
最后,为探究SENP1-NR4A1轴在体内CD8+ T细胞免疫应答中的作用,研究人员首先采用李斯特菌感染模型。与对照组相比,cKO小鼠感染后脾脏及肝脏细菌载量显著降低,CD8+ T细胞扩增增强且IFN-γ、Granzyme B及TNF-α分泌增加,表明SENP1缺失可增强CD8+ T细胞抗细菌免疫应答。进一步利用OT-I抗原特异性移植模型证实,SENP1敲低的OT-I CD8+ T细胞可显著降低受体小鼠的细菌载量,并增加抗原特异性T细胞数量,提示SENP1在抗原特异性免疫应答中发挥负向调控功能。为明确NR4A1 SUMO化修饰在该过程中的作用,研究人员在SENP1敲低的OT-I细胞中回补野生型NR4A1或SUMO化位点突变型K104R。结果显示,野生型NR4A1可部分逆转SENP1敲低所致的增强表型,而K104R突变体的回补效果更为显著,表明SENP1通过对NR4A1去SUMO化修饰抑制CD8+ T细胞介导的抗感染免疫应答。
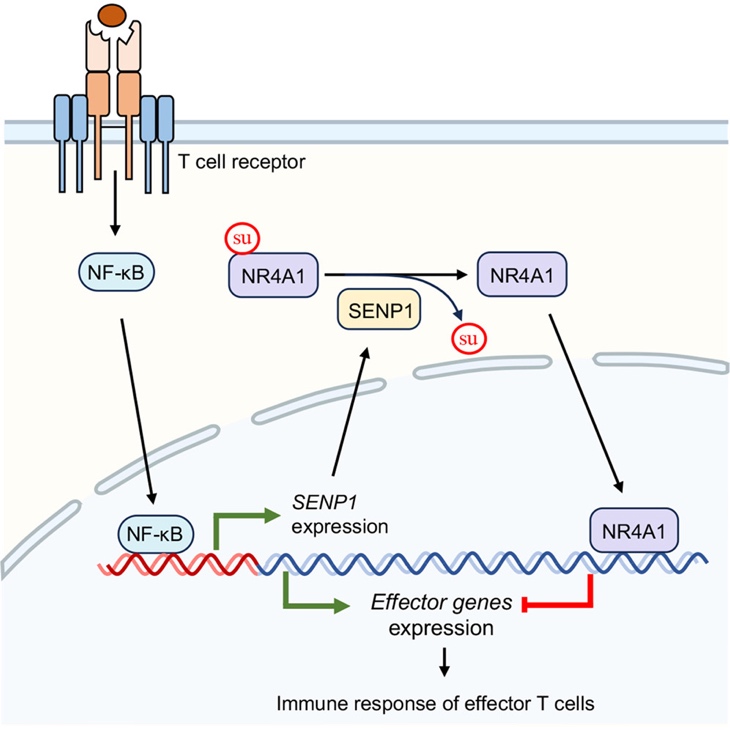
综上所述,这项研究发现了TCR信号介导的CD8+ T细胞负反馈调节机制:TCR活化通过NF-κB通路上调SENP1表达,后者经去SUMO化修饰NR4A1,限制CD8+ T细胞的应答强度,防止免疫过度激活。值得注意的是,SENP1在结直肠癌、前列腺癌及乳腺癌中表达升高,提示其可能通过抑制T细胞效应功能参与肿瘤免疫逃逸。因此,靶向T细胞中的SENP1信号轴有望成为抗肿瘤及抗病毒免疫治疗的潜在策略。
该研究论文的通讯作者为海南省医学科学院的程金科教授以及上海交通大学医学院的贺兼理副研究员(兼共同第一作者);第一作者为上海交通大学医学院江岑博士以及杨于权博士。该研究得到上海市免疫学研究所沈蕾教授、中科院生物物理研究所王盛典教授、上海交通大学医学院附属仁济医院王琦研究员、上海交通大学医学院樊秋菊老师、上海交通大学医学院田晶博士以及梁姊博士的大力支持与帮助。
原文链接:https://doi.org/10.1016/j.celrep.2026.117102


